Existe uma forma muito eficiente de produzir confusão em física clínica: recalcular o mesmo caso em dois motores, abrir DVHs lado a lado e tratar qualquer diferença como prova. Em quase todo serviço, é assim que nascem frases como “o algoritmo X calcula mais dose” ou “o algoritmo Y é mais conservador”. Quase nunca a comparação está limpa o suficiente para sustentar isso.
O motivo é simples. Quando dois resultados divergem, o que está sendo comparado não é só o nome do motor. Normalmente entram junto beam model, resolução de grade, material mapping, convenção de dose, parâmetros de MLC e até o escopo de validação daquela técnica na máquina real.
É por isso que esta parte do cluster pesa tanto na rotina. Entender AAA, Acuros XB, collapsed cone e Monte Carlo é importante. Saber comparar esses motores sem se enganar com a própria metodologia é o que realmente muda a prática.
Neste Artigo
- 1. O primeiro erro: achar que algoritmo é igual a resultado
- 2. Beam model: a parte invisível da comparação
- 3. O segundo erro: comparar grids diferentes como se fossem a mesma coisa
- 4. O terceiro erro: ignorar a convenção de dose
- 5. O quarto erro: tratar a técnica como se fosse automaticamente validada
- 6. O que commissioning realmente deveria responder
- 7. Uma matriz de testes é melhor do que uma pilha de medições desconectadas
- 8. O papel dos fantomas heterogêneos
- 9. Gamma não resolve tudo
- 10. QA por paciente não substitui QA do algoritmo
- 11. Quando a comparação entre algoritmos é realmente útil
- 12. Um roteiro mínimo para comparar algoritmos com rigor
- 13. O que a literatura e os manuais ensinam em conjunto
- 14. O ganho real de uma comparação bem feita
O primeiro erro: achar que algoritmo é igual a resultado
O algoritmo importa muito, mas ele nunca trabalha sozinho. Em qualquer TPS comercial sério, o resultado que aparece na tela depende de pelo menos cinco camadas:
- modelo de feixe (beam model);
- dados de commissioning e medição;
- resolução e discretização;
- representação do paciente e dos materiais;
- convenção de reporte da dose.
Quando alguém diz que “o algoritmo X deu dose maior que o algoritmo Y”, a frase está incompleta. O que deu dose maior foi um conjunto inteiro de escolhas: motor, modelo, grid, material mapping, técnica, máquina e, às vezes, grandeza de dose diferente.
Beam model: a parte invisível da comparação
O beam model é um dos fatores mais subestimados em comparações entre TPS. Ele define como o sistema descreve:
- a fonte primária;
- fótons extra-focais;
- contaminação eletrônica;
- colimadores;
- MLC;
- wedges;
- fatores de saída;
- parâmetros geométricos e dosimétricos do feixe.
O Eclipse deixa isso evidente ao mostrar que AAA e Acuros XB compartilham o mesmo photon beam source model. Já o RayStation insiste, em seu IFU, que certos cenários, especialmente small field rotational plans, são altamente sensíveis a parâmetros de MLC do beam model.
Essa observação é decisiva. Às vezes, o físico acredita estar vendo uma diferença de família algorítmica, quando na verdade está vendo:
- diferença de MLC modeling;
- diferença de commissioning;
- diferença de parametrização de fonte.
Sem isolar essas camadas, a comparação vira mistura de causas.
O segundo erro: comparar grids diferentes como se fossem a mesma coisa
Resolução de dose não é detalhe cosmético. Ela muda:
- amostragem de gradiente;
- definição da penumbra;
- dose em volumes pequenos;
- comportamento em interfaces;
- aparência do acordo entre algoritmos.
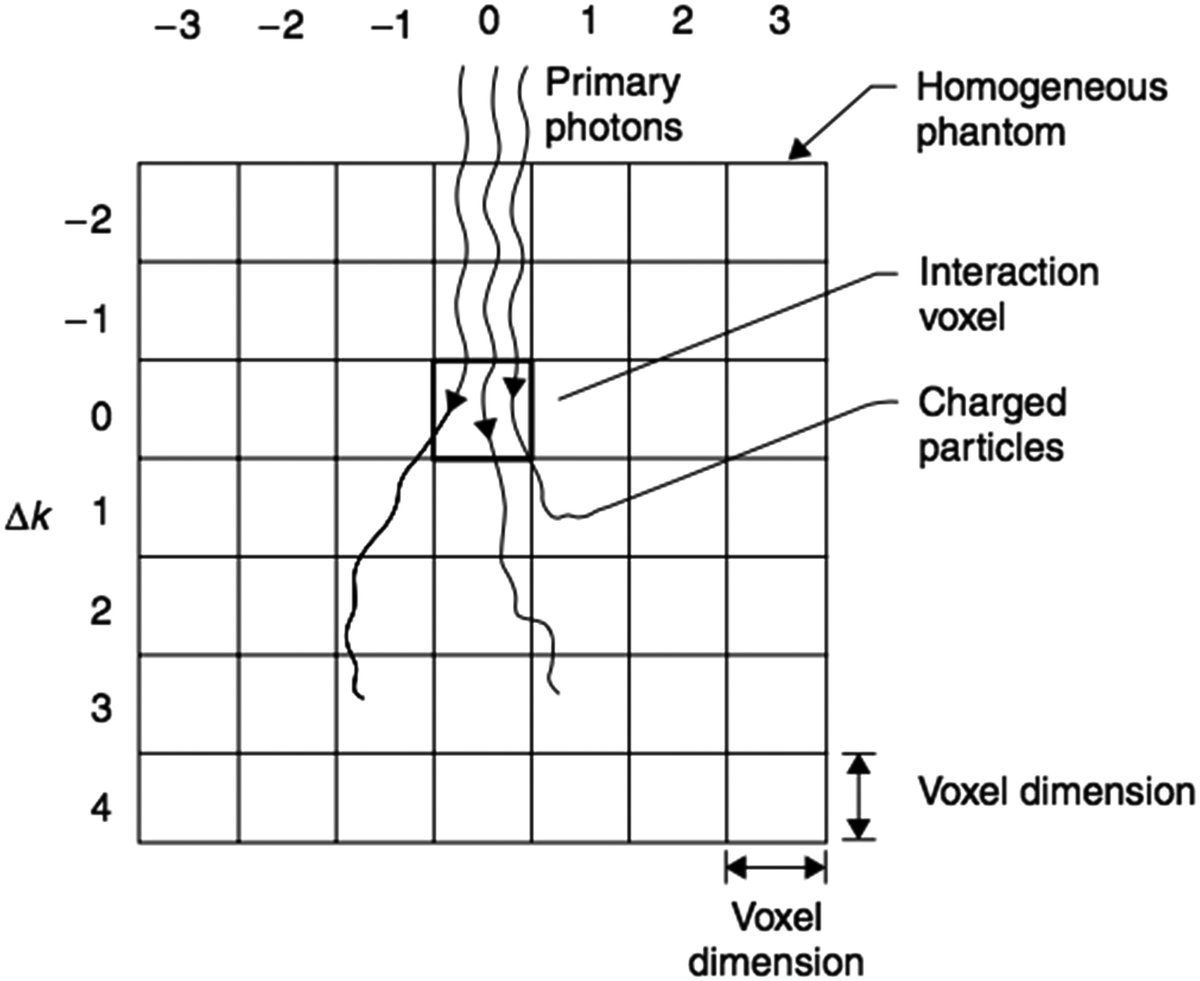
O AAA usa grade divergente internamente e depende da relação entre resolução escolhida, pixel spacing e separação entre cortes. O Acuros XB usa discretização espacial variável com refinamento adaptativo. Monte Carlo, por sua vez, ainda traz o componente adicional do ruído estatístico por voxel.
Isso significa que comparar dois algoritmos sem equalizar a malha de saída, ou sem ao menos entender como cada um discretiza o problema internamente, é metodologicamente frágil.
Uma regra prática útil é esta: antes de discutir física, alinhe discretização.
O terceiro erro: ignorar a convenção de dose
Esse ponto fica cada vez mais importante à medida que os serviços passam a usar algoritmos material-explícitos.
O Acuros XB permite dose to medium e dose to water. O RayStation, no material local, alerta que o photon collapsed cone computa dose para água, enquanto o photon Monte Carlo reporta dose para meio. O mesmo documento adverte explicitamente sobre o risco de combinar ou comparar distribuições de motores diferentes quando o caso é sensível a materiais de alto Z.
Se o serviço ignora isso, o que parece divergência algorítmica pode ser, em parte, divergência de grandeza física reportada.
Em termos práticos, antes de comparar qualquer dose entre motores, o físico precisa responder:
- os dois motores estão reportando a mesma convenção?
- a diferença esperada entre as convenções é pequena neste material?
- há osso, implante ou outro material que amplifique essa discrepância?
Sem essas perguntas, até um DVH bonito pode estar sendo interpretado de forma errada.
O quarto erro: tratar a técnica como se fosse automaticamente validada
O IFU do RayStation é muito útil porque fala a linguagem que todo serviço deveria adotar. O documento lembra que certas técnicas, como VMAT sequencing, devem ser tratadas como praticamente uma nova técnica, exigindo:
- validação do beam model;
- validação do comportamento da máquina;
- QA por paciente.
Essa observação deveria ser universalizada. O fato de um algoritmo funcionar muito bem em 3D-CRT não garante automaticamente o mesmo comportamento em:
- IMRT fixa;
- VMAT;
- wave arcs;
- campos muito pequenos;
- técnicas específicas de plataforma.
Sempre que a técnica muda, a validade do conjunto algoritmo + beam model + entrega precisa ser reavaliada.
O que commissioning realmente deveria responder
Em vez de tratar commissioning como checklist genérico, vale formular as perguntas certas.
Um commissioning sério precisa mostrar:
- se o motor reproduz profundidade dose, perfis e fatores de saída da máquina;
- se o comportamento se mantém em campos pequenos;
- se o algoritmo responde corretamente em meios heterogêneos relevantes para a clínica local;
- se a modelagem de MLC está adequada;
- se as escolhas de grid e de imagem não introduzem artefatos relevantes;
- se a convenção de dose adotada é conhecida e consistente.
Em outras palavras, commissioning não é “fazer o algoritmo passar”. É descobrir em que território aquele conjunto pode ser usado com confiança.
Uma matriz de testes é melhor do que uma pilha de medições desconectadas
Em vez de pensar commissioning como coleção de dados, vale pensar como matriz de perguntas. Uma matriz mínima útil costuma cruzar:
- campo aberto e campo pequeno;
- homogêneo e heterogêneo;
- eixo central e fora do eixo;
- técnica simples e técnica modulada;
- material água-equivalente e material clinicamente desafiador.
Quando a equipe monta essa matriz, fica mais fácil perceber se o algoritmo está falhando em uma fronteira específica do uso clínico ou se o problema é global. Sem essa organização, o serviço pode ter muitas medições e pouca clareza.
O papel dos fantomas heterogêneos
Heterogeneidade não pode ser deixada apenas para o caso clínico real. Quando um serviço pretende usar algoritmos mais sofisticados justamente por causa de pulmão, osso, cavidades ou implantes, precisa testar o conjunto em geometrias que obriguem o motor a lidar com esses fenômenos.
Os materiais locais usados aqui reforçam essa necessidade:
- o Eclipse explicita limitações em pulmão;
- o RayStation descreve validações em geometrias homogêneas e heterogêneas, inclusive com IAEA test suite, AAPM TG105 e comparação com EGSnrc;
- o handbook mostra benchmarks em que a diferença entre AAA e Acuros XB aparece de forma clara em heterogeneidades de baixa densidade.
Isso sugere uma regra simples: se o serviço quer se apoiar em ganho de performance em heterogeneidade, precisa validar heterogeneidade com intenção, não por inferência.
Gamma não resolve tudo
Gamma continua útil, mas é frequentemente usado como atalho mental. Um motor pode passar em gamma global e ainda esconder diferenças clinicamente relevantes em regiões pequenas, interfaces ou materiais específicos.
O RayStation usa critérios como 95% dos pontos com gamma 3%, 3 mm < 1, e isso faz sentido como parte do processo de validação. Mas a leitura madura não para aí. Um conjunto de testes precisa combinar:
- gamma;
- diferenças pontuais;
- leitura de perfis;
- atenção a regiões de gradiente;
- análise em heterogeneidades;
- interpretação clínica do local da discrepância.
Se o gamma passa, mas a diferença relevante está exatamente no pulmão distal, no osso ou junto a um implante, o problema não desaparece.
QA por paciente não substitui QA do algoritmo
Outro equívoco frequente é usar QA por paciente como se ele pudesse compensar qualquer lacuna no entendimento do motor de dose. Não pode.
QA por paciente responde, em geral, a uma pergunta mais restrita: se o plano calculado e entregue mantém coerência dentro de um arranjo específico de medição e critério de comparação.
Ele não substitui:
- validação do algoritmo em heterogeneidade;
- entendimento da convenção de dose;
- análise do beam model;
- escopo formal de commissioning da técnica.
Quando o serviço usa QA por paciente como muleta para uma dúvida algorítmica estrutural, ele corre o risco de validar repetidamente a mesma hipótese frágil.
Quando a comparação entre algoritmos é realmente útil
Comparar motores faz sentido quando a instituição quer responder perguntas concretas, por exemplo:
- AAA e Acuros XB mudam a cobertura em pulmão pequeno de alta energia?
- o CC e o MC do RayStation divergem em um sítio com osso ou alto Z?
- a mudança de motor altera interpretação de background dose ou reirradiação?
- a diferença observada pertence ao transporte ou à convenção de dose?
Essa é a comparação boa: orientada por hipótese.
A comparação ruim é a que busca provar, de forma genérica, que “algoritmo A é melhor que algoritmo B” sem declarar cenário, técnica, material e beam model.
Um roteiro mínimo para comparar algoritmos com rigor
Se a instituição quiser fazer isso direito, um roteiro mínimo inclui:
- igualar ou justificar grid e imagem;
- verificar se os beam models estão maduros;
- declarar a convenção de dose de cada motor;
- separar testes homogêneos de testes heterogêneos;
- incluir ao menos um cenário clinicamente crítico para o serviço;
- avaliar perfis, profundidade, dose local e não só DVH;
- registrar em que situações a diferença muda decisão e em quais não muda.
Esse roteiro já filtra boa parte do ruído metodológico que costuma aparecer em discussões informais sobre TPS.
O que a literatura e os manuais ensinam em conjunto
Lendo lado a lado os documentos locais usados neste cluster, aparece uma mensagem convergente.
O Eclipse mostra que algoritmos diferentes têm fundamentos diferentes e limitações conhecidas. O RayStation mostra que motores distintos convivem com escopos de validação específicos e convenções de dose potencialmente diferentes. O handbook mostra que o desempenho relativo entre famílias algorítmicas muda de acordo com a heterogeneidade e a física dominante do caso.
Juntos, esses materiais deixam uma conclusão incômoda, mas importante: se a comparação entre algoritmos foi feita sem declarar o restante da cadeia de modelagem, a conclusão provavelmente está superinterpretada.
O ganho real de uma comparação bem feita
Quando a comparação é bem montada, ela deixa de produzir slogans e começa a produzir fronteiras de confiança. Ou seja:
- em quais cenários o algoritmo A já é suficiente;
- em quais cenários vale recalcular com B;
- em quais cenários a diferença observada é física de fato;
- em quais cenários ela é apenas metodológica.
Esse tipo de resposta vale mais para a clínica do que qualquer ranking genérico entre TPS. No fim, é isso que um commissioning decente deveria entregar: não um “algoritmo vencedor”, mas um mapa honesto de onde cada combinação motor + beam model + técnica ainda responde bem e onde ela já precisa de validação extra, recalculação ou mudança de estratégia.