Collapsed Cone Convolution: a física por trás do cálculo de dose moderno
O algoritmo Collapsed Cone Convolution (CCC) representa um dos avanços mais significativos no cálculo de dose para radioterapia por fótons. Desenvolvido por Ahnesjö em 1989, o CCC resolve um problema prático que desafiava os físicos médicos: como calcular dose com precisão em meios heterogêneos sem o custo computacional proibitivo da superposição completa ponto a ponto? A resposta está na combinação inteligente de kernels de deposição de energia com uma aproximação geométrica que colapsa a energia transportada em cones discretos. Para uma visão completa dos algoritmos de cálculo de dose, desde os métodos empíricos até Monte Carlo, confira nosso guia completo sobre algoritmos de cálculo de dose por fótons.
Neste artigo, apresentamos uma análise exaustiva dos três artigos fundamentais que definiram o CCC: os kernels de deposição de energia gerados por Monte Carlo (Mackie et al., 1988), o método de convolução com cones colapsados (Ahnesjö, 1989) e a implementação prática em sistema de planejamento (Cho et al., 2012). Também discutiremos as implementações comerciais em sistemas como Pinnacle (Philips), Oncentra (Elekta) e RayStation (RaySearch), e compararemos o CCC com outros algoritmos de cálculo de dose.
Neste Artigo
- 1. Contexto Histórico: Por Que o CCC Foi Necessário
- 2. Mackie 1988: Kernels Monte Carlo com EGS
- 3. Representação Analítica e Kernels Polienergéticos
- 4. Ahnesjö 1989: O Método Collapsed Cone
- 5. Divergência do Feixe e Inclinação dos Kernels
- 6. Scaling por Densidade e Heterogeneidades
- 7. Cho 2012: Implementação Prática com Modelo de Três Fontes
- 8. Implementações Comerciais em TPS
- 9. Tabela Comparativa: CCC vs Pencil Beam vs AAA vs Monte Carlo
- 10. Limitações e Situações Críticas
- 11. Considerações Finais
Contexto Histórico: Por Que o CCC Foi Necessário
Nos anos 1980, o cálculo de dose para radioterapia dependia de métodos empíricos baseados em tabelas de porcentagem de dose profunda (PDD) e perfis laterais medidos em água. Esses métodos — como o algoritmo de Clarkson para integração de campos irregulares — funcionavam razoavelmente para geometrias simples em meios homogêneos, mas não conseguiam lidar com a realidade anatômica dos pacientes. Tecido pulmonar, cavidades de ar, osso cortical e implantes metálicos alteram profundamente o transporte de radiação, e os métodos empíricos aplicavam apenas correções grosseiras de razão tecido-ar (TAR) ou razão tecido-fantoma (TPR).
O problema fundamental era conceitual. Em um meio homogêneo de água, a dose em qualquer ponto pode ser calculada por convolução: a fluência de fótons primários é convolvida com um kernel que descreve como a energia se redistribui após cada interação. Mackie et al. (1985) formalizaram isso matematicamente. Porém, em meios heterogêneos, o kernel muda de ponto para ponto — dependendo da densidade e composição do tecido entre o ponto de interação e o ponto de deposição. A convolução simples se transforma em superposição, e o custo computacional sobe de $n^3$ para $n^6$ operações, onde $n$ é o número de voxels por dimensão.
A simulação Monte Carlo completa resolvia o problema com precisão, porém em 1989 um planejamento típico levaria horas ou dias no hardware disponível. Os clínicos precisavam de algo intermediário: um algoritmo que capturasse a física do transporte de energia em meios heterogêneos, mas que rodasse em minutos. O CCC de Ahnesjö preencheu essa lacuna com uma solução elegante — reduzindo a complexidade para $n^4 \times m$ operações através da aproximação de cones colapsados, sem sacrificar significativamente a precisão dosimétrica.
Mackie 1988: Geração de Kernels por Monte Carlo com EGS
Os kernels de deposição de energia — também chamados de energy deposition point kernels ou dose spread arrays — são a peça central de qualquer algoritmo de convolução/superposição. Eles descrevem como a energia se distribui no espaço ao redor de um ponto de interação primária de fótons. O trabalho seminal de T.R. Mackie, J.W. Scrimger, J.J. Battista (1988) estabeleceu o método padrão para gerar esses kernels usando simulação Monte Carlo.
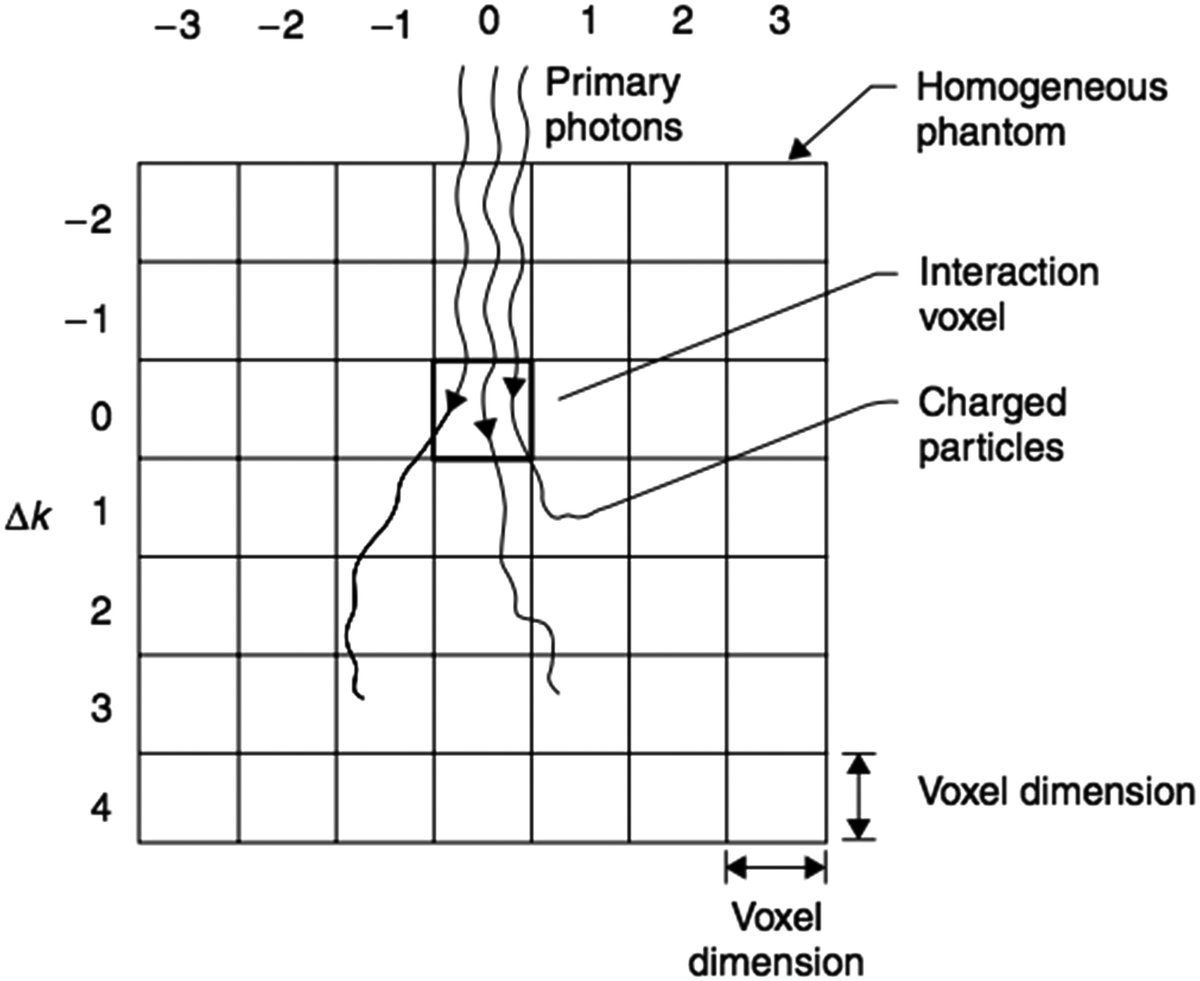
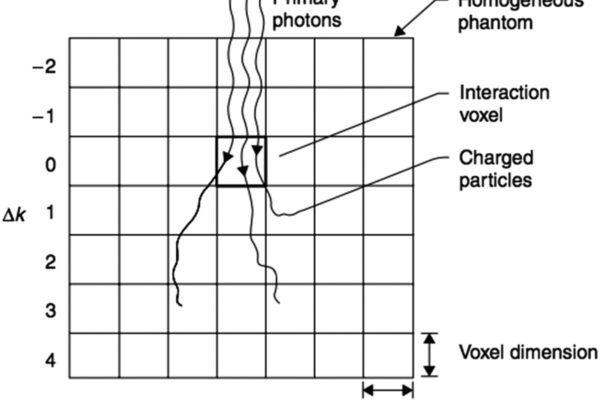
Geometria de simulação
Mackie e colaboradores utilizaram o código Monte Carlo EGS (Electron Gamma Shower) com um código de usuário chamado SCASPH para simular o transporte de partículas em um fantoma esférico homogêneo de água. A geometria era dividida em:
- Cones angulares de 3,75° de abertura (48 cones cobrindo 180°)
- 24 cascas radiais concêntricas com espaçamentos crescentes
- Interação forçada no centro exato da esfera
Fótons monoenergéticos eram forçados a interagir no centro da esfera. A partir dessa interação primária, todas as partículas secundárias — elétrons Compton, pares elétron-pósitron, fotoelétrons, elétrons de aniquilação e fótons de bremsstrahlung — eram rastreadas até perder toda sua energia cinética ou escapar do fantoma. A energia depositada em cada voxel (definido pela interseção cone-casca) era registrada e acumulada ao longo de milhares de histórias.
Kernels para diferentes ordens de espalhamento
Uma contribuição fundamental do trabalho de Mackie foi a decomposição dos kernels por ordem de espalhamento:
- Kernel primário ($K_p$): energia depositada por partículas carregadas geradas na interação primária (Compton, efeito fotoelétrico, produção de pares)
- Kernel de primeiro espalhamento ($K_{s1}$): energia depositada após uma única interação de espalhamento do fóton secundário
- Kernel de segundo espalhamento ($K_{s2}$): após duas interações de espalhamento
- Kernel de espalhamento múltiplo ($K_{sm}$): todas as ordens superiores
- Kernel de bremsstrahlung e aniquilação ($K_{ba}$): fótons gerados por esses processos
Os kernels foram calculados para fótons monoenergéticos de 0,1 a 50 MeV. Além dos kernels de deposição, o trabalho também caracterizou o transporte de partículas primárias por parâmetros como centro efetivo do voxel, profundidade de penetração, raio efetivo e distância lateral efetiva. Esses dados serviram como banco de dados fundamental para todos os algoritmos de convolução/superposição subsequentes, incluindo o CCC.
Integrais de normalização
O kernel total pode ser decomposto em componentes primária e de espalhamento. As integrais de normalização satisfazem:
$$\iiint K_p(\mathbf{r})\,dV = \frac{\mu_{en}}{\mu}$$
$$\iiint K_s(\mathbf{r})\,dV = \frac{\mu – \mu_{en}}{\mu}$$
Onde $\mu$ é o coeficiente de atenuação linear total e $\mu_{en}$ é o coeficiente de absorção linear de energia. Essas relações são fundamentais para verificação dos kernels gerados e para aplicação de correções de qualidade do feixe em implementações clínicas.
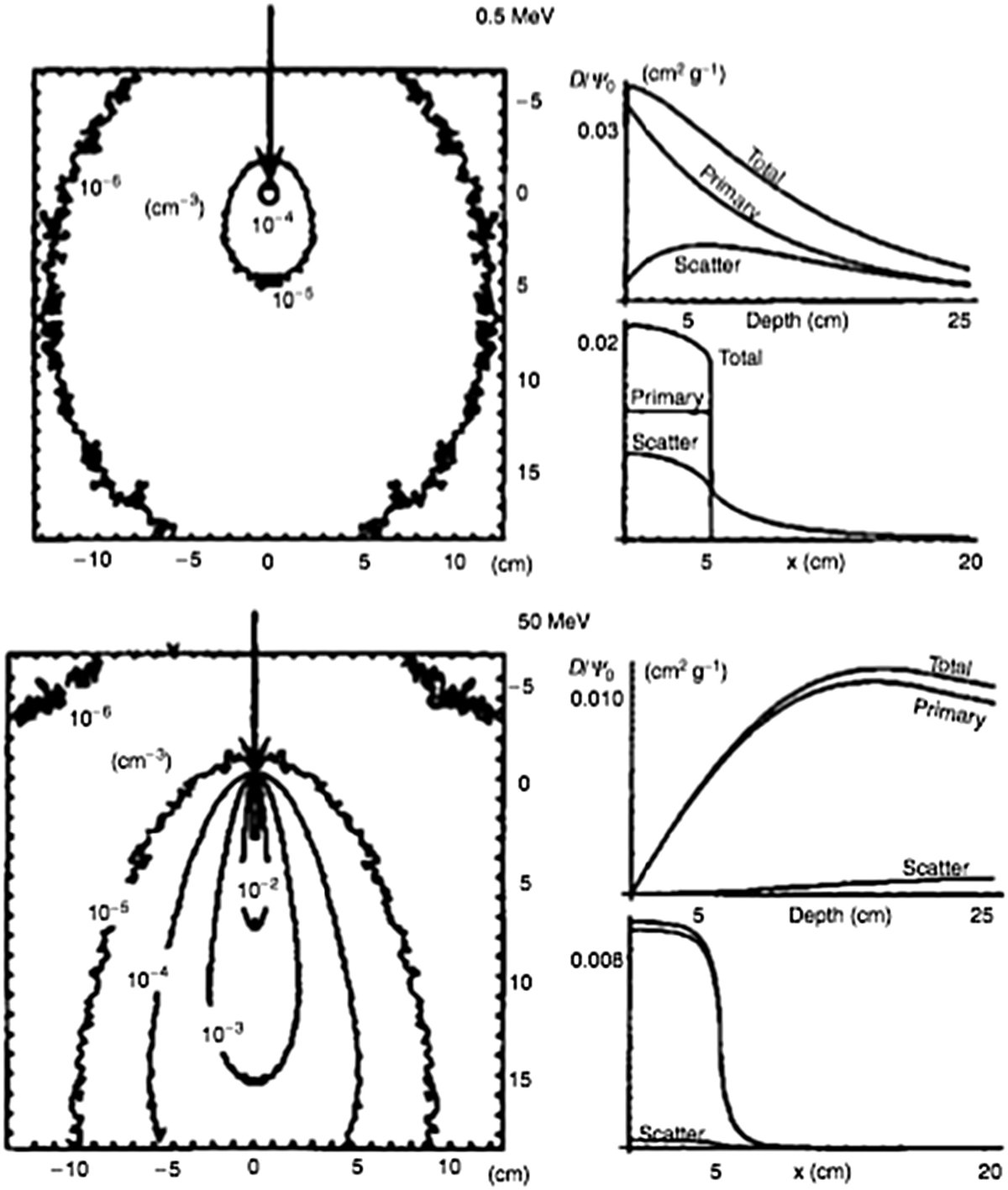
Dependência com a energia
A figura ao lado ilustra kernels para 0,5 MeV e 50 MeV. A diferença é dramática. Em baixas energias (abaixo de 1 MeV), a contribuição de fótons espalhados domina e o kernel é relativamente isotrópico — a energia se distribui quase uniformemente em todas as direções. Em altas energias (acima de 10 MeV), o transporte de elétrons torna-se dominante e altamente direcional: a energia é depositada preferencialmente na direção forward (mesma direção do fóton incidente), com alcances laterais significativos dos elétrons secundários.
Essa mudança de comportamento com a energia tem consequências práticas profundas. Para feixes de 6 MV, onde o espectro médio está em torno de 2 MeV, os kernels são moderadamente anisotrópicos e a correção por heterogeneidades tem importância intermediária. Para feixes de 15-18 MV, os kernels são fortemente anisotrópicos e as falhas de algoritmos simples em pulmão e cavidades de ar tornam-se clinicamente relevantes. O CCC, por transportar energia ao longo de direções discretas com scaling por densidade, captura essa anisotropia de forma significativamente melhor que algoritmos do tipo pencil beam.
Representação Analítica e Kernels Polienergéticos
Trabalhar diretamente com kernels tabulados para cada energia em cada ângulo é computacionalmente caro e dificulta o cálculo recursivo. Ahnesjö e Mackie (1987) propuseram um ajuste analítico que viabilizou o CCC:
$$K(r, \theta) = \frac{A_\theta\, e^{-a_\theta r} + B_\theta\, e^{-b_\theta r}}{r^2}$$
Onde:
- $r = |\mathbf{r} – \mathbf{r}’|$ é a distância entre o ponto de interação $\mathbf{r}’$ e o ponto de deposição $\mathbf{r}$
- $\theta$ é o ângulo em relação à direção do fóton incidente
- $A_\theta, a_\theta, B_\theta, b_\theta$ são parâmetros de ajuste que dependem de $\theta$ e do espectro energético
- O fator $1/r^2$ compensa a dispersão geométrica a partir de uma fonte pontual
- O primeiro exponencial descreve principalmente a deposição primária (curto alcance); o segundo, a componente de espalhamento (longo alcance)
A beleza desta formulação está na possibilidade de cálculo recursivo. Se conhecemos a dose acumulada até a posição $r_i$ ao longo de uma linha, a contribuição até $r_{i+1} = r_i + \Delta r$ pode ser obtida multiplicando pela exponencial correspondente — sem recalcular toda a integral. Essa propriedade é o que torna o CCC computacionalmente viável.
Kernels polienergéticos para feixes clínicos
Feixes clínicos não são monoenergéticos. Um feixe de 6 MV contém fótons de 0 a 6 MeV com energia média em torno de 2 MeV. Além disso, o espectro muda com a profundidade (endurecimento do feixe) e com a posição lateral (amolecimento fora do eixo). Existem duas abordagens principais:
- Soma ponderada pelo espectro: kernels polienergéticos são gerados por soma ponderada dos kernels monoenergéticos de Mackie, usando os pesos do espectro de fluência incidente. É o método mais direto.
- Interpolação por profundidade: Liu et al. (1997) propuseram pré-calcular kernels polienergéticos em três profundidades distintas (raso, intermediário, profundo) e interpolar entre eles durante o cálculo. Isso compensa automaticamente o endurecimento do feixe sem necessidade de recalcular o espectro em cada ponto.
Uma alternativa refinada consiste em convolver separadamente os kernels primário e de espalhamento com as respectivas frações TERMA: $\mu_{en}/\mu$ para o primário e $(\mu – \mu_{en})/\mu$ para o espalhamento. Como cada componente é afetada de forma diferente pela mudança espectral, essa separação melhora a precisão sem custo computacional significativo.
Ahnesjö 1989: O Método Collapsed Cone Convolution
O artigo de Anders Ahnesjö, publicado em 1989 na revista Medical Physics, é o trabalho fundador do CCC. Ahnesjö propôs uma solução elegante para o problema da superposição em meios heterogêneos, combinando três inovações: ray-tracing para TERMA, kernels polienergéticos analíticos e a aproximação de cone colapsado.
Cálculo da TERMA por ray-tracing
A TERMA (Total Energy Released per unit MAss) descreve a energia total liberada por fótons em cada ponto do volume. Ahnesjö calculou a TERMA traçando raios desde a fonte de fótons através do volume do paciente:
$$T(\mathbf{r}’) = \Psi(\mathbf{r}’) \cdot \frac{\mu(\mathbf{r}’)}{\rho(\mathbf{r}’)}$$
Onde $\Psi(\mathbf{r}’)$ é a fluência energética no ponto $\mathbf{r}’$ (calculada pelo ray-tracing com atenuação exponencial) e $\mu/\rho$ é o coeficiente mássico de atenuação do tecido naquele ponto. A fluência é atenuada ao longo do caminho considerando a composição e densidade do tecido — heterogeneidades como pulmão, osso e ar alteram tanto a atenuação quanto a TERMA resultante.
A aproximação de cone colapsado
A superposição direta requer integrar a contribuição de todos os $n^3$ voxels de interação para cada um dos $n^3$ voxels de deposição — $n^6$ operações no total, subindo para $n^7$ com scaling variável. O CCC resolve isso discretizando o espaço angular em $m$ direções fixas (tipicamente 13 eixos gerando 26 sentidos, ou versões mais refinadas com 48 ou mais direções).

Para cada uma dessas $m$ direções, toda a energia de um cone sólido com ângulo sólido $\Omega$ é colapsada (projetada) sobre a linha central do cone. A energia é então transportada e depositada passo a passo ao longo dessa linha, usando a formulação analítica do kernel. Em cada passo, o cálculo considera a densidade radiológica local para escalar o kernel.
A equação de deposição ao longo de uma direção de cone $\hat{\Omega}_j$ pode ser escrita como:
$$D_j(\mathbf{r}) = \sum_{i} T(\mathbf{r}_i’) \cdot \Delta V_i \cdot \frac{\Omega_j}{4\pi} \cdot \frac{A_\theta e^{-a_\theta d_{\rho}} + B_\theta e^{-b_\theta d_{\rho}}}{d_{\rho}^2}$$
Onde $d_{\rho}$ é a distância radiológica (escalada pela densidade) entre $\mathbf{r}_i’$ e $\mathbf{r}$, e $\Omega_j/4\pi$ é a fração do ângulo sólido coberta pelo cone $j$. A dose total é a soma sobre todas as direções:
$$D(\mathbf{r}) = \sum_{j=1}^{m} D_j(\mathbf{r})$$
Graças à forma exponencial dos kernels, o transporte ao longo de cada linha pode ser calculado recursivamente. Se designarmos por $E_j(\mathbf{r}_k)$ a energia acumulada que chega ao voxel $k$ ao longo da direção $j$, a contribuição do voxel seguinte $k+1$ pode ser obtida por:
$$E_j(\mathbf{r}_{k+1}) = E_j(\mathbf{r}_k) \cdot e^{-a_\theta \Delta d_{\rho}} + T(\mathbf{r}_k) \cdot \Delta V_k \cdot \frac{\Omega_j}{4\pi}$$
Essa recursão reduz o número total de operações para $n^4 \times m$, onde $n^3$ são os voxels e $n$ é o comprimento típico das linhas de transporte. Na prática, com $m \sim 26$ a $48$ direções e grids de $128^3$ a $256^3$ voxels, o cálculo completo leva de segundos a poucos minutos em hardware moderno.
Conservação de energia no CCC
A aproximação de cone colapsado preserva a conservação de energia por construção. Toda a energia emitida em cada ângulo sólido é atribuída à linha central do cone correspondente. Não há perda nem ganho líquido — a energia total depositada no volume é igual à energia total liberada (TERMA integrada), respeitando as frações de escape quando a energia sai do volume do paciente.
Validação original
Ahnesjö validou o CCC para potenciais de aceleração de 4, 6, 10, 15 e 24 MeV em duas geometrias:
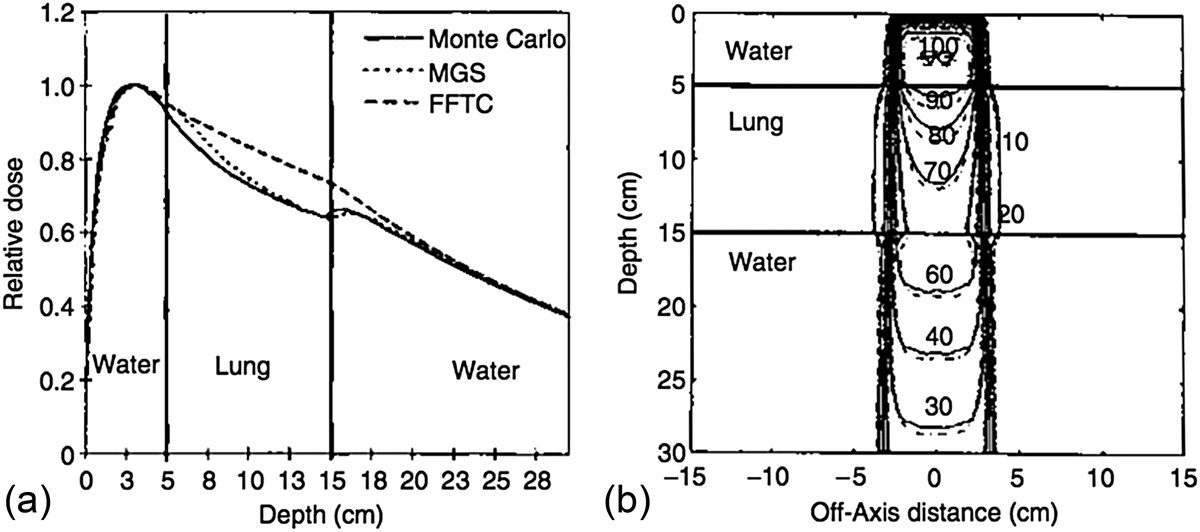
- Pilha de camadas de tecidos: água + pulmão + água, testando a capacidade do CCC de lidar com interfaces de densidade
- Fantoma mediastinal: cortiça (simulando pulmão) e água, reproduzindo uma geometria clinicamente relevante
As distribuições de dose calculadas pelo CCC foram comparadas com simulações de referência usando o código Monte Carlo EGS4. A concordância foi excelente em ambas as geometrias e em toda a faixa de energia testada. Ahnesjö demonstrou que o número de operações é proporcional ao número de pontos de cálculo — viabilizando o uso clínico rotineiro. O artigo original observa que o CCC é capaz de modelar tanto o transporte lateral de elétrons em interfaces quanto a atenuação diferencial em meios de densidades distintas, superando os algoritmos baseados em correção primário-espalhamento que estavam disponíveis na época.
Divergência do Feixe e Inclinação dos Kernels
Um feixe clínico real diverge a partir da fonte. Essa divergência modifica não apenas a fluência (lei do inverso do quadrado), mas também a direção dos kernels: rigorosamente, kernels fora do eixo devem ser inclinados para acompanhar a divergência. Na prática, Sharpe e Battista (1993) mostraram que, para a maioria dos casos clínicos, manter os kernels paralelos ao eixo central é aceitável.
Quando isso deixa de funcionar? Em distâncias fonte-superfície curtas, campos grandes e altas energias. Substituir um kernel inclinado por um paralelo aumenta sua contribuição ao eixo do feixe, superestimando o PDD on-axis. Papanikolaou et al. (1993) e Liu et al. (1997) propuseram como compensação aplicar a correção do inverso do quadrado nos pontos de deposição em vez de nos pontos de interação primária. Ahnesjö et al. (2005) adotaram uma abordagem mais explícita: usar a forma analítica dos kernels com parâmetros de ajuste dependentes do ângulo de inclinação.
Scaling por Densidade e Heterogeneidades Teciduais
O tratamento de heterogeneidades é onde o CCC se diferencia fundamentalmente dos algoritmos mais simples. Se o meio tem densidade diferente da água, o teorema de O’Connor permite obter a mesma distribuição de dose escalando todas as dimensões do fantoma proporcionalmente. Na prática, isso equivale a substituir todas as distâncias na equação de convolução pelas distâncias radiológicas equivalentes.
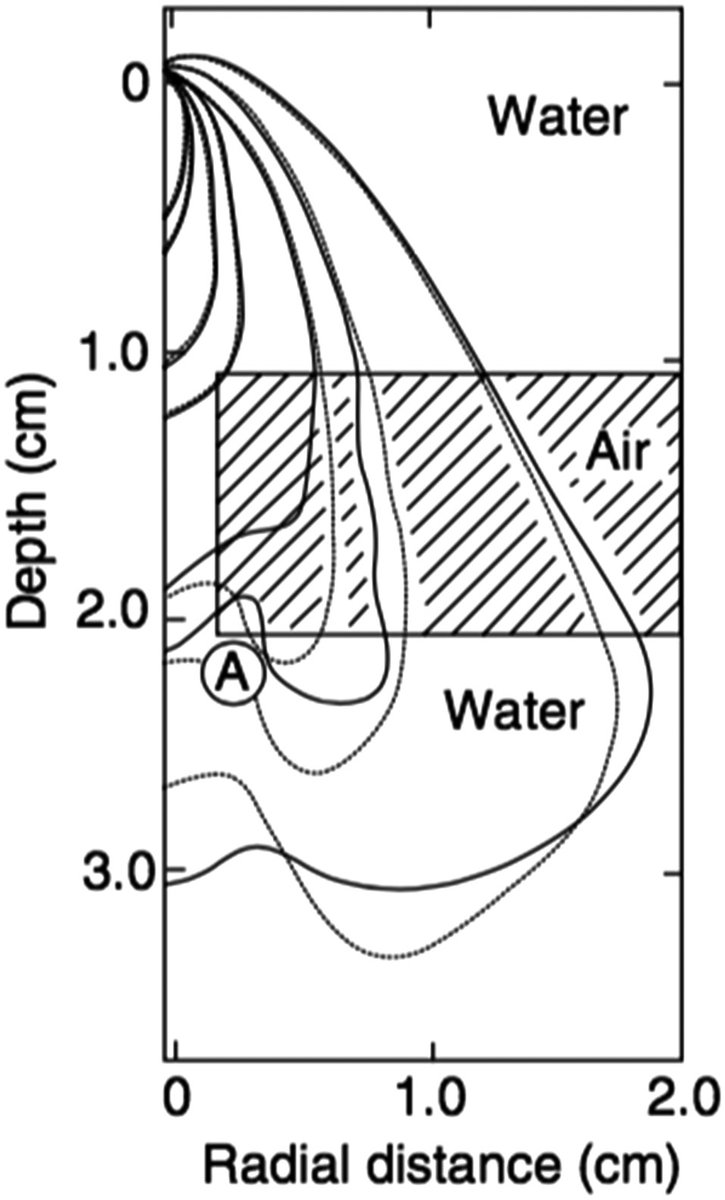
A equação geral de convolução em meio homogêneo é:
$$D(\mathbf{r}) = \iiint T(\mathbf{r}’) \cdot K(\mathbf{r} – \mathbf{r}’)\,d^3\mathbf{r}’$$
Em meios heterogêneos, as distâncias são escaladas conforme a densidade local. Devemos considerar separadamente:
- A densidade $\rho_1$ entre a superfície e $\mathbf{r}’$ — que modifica a fluência $\Psi(\mathbf{r}’)$ e portanto a TERMA
- A densidade do meio em $\mathbf{r}’$ — que modifica a TERMA via $\mu/\rho$
- A densidade $\rho_2$ entre $\mathbf{r}’$ e $\mathbf{r}$ — que modifica o kernel para $K(\rho_2 \cdot |\mathbf{r} – \mathbf{r}’|)$
No CCC, esse scaling é aplicado naturalmente ao longo de cada linha de transporte. A distância radiológica $d_\rho$ acumula a densidade relativa voxel a voxel: $d_\rho = \sum_i \rho_i \cdot \Delta s_i$, onde $\Delta s_i$ é o comprimento geométrico no voxel $i$ e $\rho_i$ é sua densidade relativa à água. Essa acumulação permite que o kernel exponencial se ajuste automaticamente: em pulmão ($\rho \approx 0,3$), a distância radiológica cresce mais lentamente que a distância geométrica, fazendo com que o kernel decaia mais lentamente e a energia penetre mais profundamente — exatamente o que acontece na realidade física.
Mesmo com scaling completo, a equação de convolução em meio heterogêneo permanece aproximada. Para o kernel primário, o scaling retilíneo não é exato quanto ao espalhamento múltiplo de elétrons secundários. Para o kernel de espalhamento, o scaling retilíneo só é rigoroso para a componente de primeiro espalhamento. Mackie et al. (1985) sugeriram separar o kernel de primeiro espalhamento do de espalhamento múltiplo, escalando este último com base em uma densidade média. Como a componente de espalhamento múltiplo é uma fração pequena da dose total — especialmente em alta energia — usar o mesmo valor de densidade para todo o espalhamento também é aceitável na prática clínica.
Cho 2012: Implementação Prática com Modelo de Três Fontes
O artigo de Woong Cho, Kwangzoo Chung e colaboradores (2012), publicado no Journal of the Korean Physical Society, detalha como transformar a teoria do CCC em um sistema de planejamento funcional. Enquanto Ahnesjö definiu o framework matemático, Cho demonstrou os detalhes práticos da implementação.
Modelo de fluência com três fontes
O primeiro desafio prático é determinar a fluência de fótons que entra no paciente. Cho utilizou um modelo de três fontes:
- Fonte principal (target): fótons de bremsstrahlung gerados no alvo do acelerador linear. A distribuição angular e energética é caracterizada por parâmetros ajustados a partir de medidas de PDD e perfis em água.
- Espalhamento pelo colimador primário: fótons que interagem com as mandíbulas e o colimador primário antes de atingir o paciente. Contribuem para o alargamento da fluência fora do campo definido.
- Espalhamento adicional pelo cabeçote (gantry): fótons espalhados pelo filtro equalizador, bandeja de acessórios e outras estruturas do cabeçote. Contribuem para a dose fora do campo e para a forma dos perfis laterais.
Esse modelo de múltiplas fontes é mais preciso que o modelo de fonte pontual simples, especialmente para campos grandes e para reproduzir o efeito horn (aumento da fluência nas bordas do campo causado pelo filtro equalizador). Os parâmetros do modelo são ajustados durante o commissioning do acelerador, usando medidas de PDD, perfis laterais e fatores de output para diferentes tamanhos de campo.
Cálculo da TERMA com efeitos físicos
A TERMA no trabalho de Cho incorpora vários efeitos físicos que são ignorados em implementações simplificadas:
- Espectro polienergético: a atenuação é calculada usando coeficientes dependentes da energia, ponderados pelo espectro local
- Efeito horn: a variação radial da fluência causada pelo filtro equalizador cônico
- Amolecimento do feixe (beam softening): a energia média do espectro diminui fora do eixo e aumenta com a profundidade
- Transmissão por MLC: a atenuação pelas lâminas do colimador multilâmina, incluindo transmissão interleaf e tongue-and-groove
- Atenuação no meio: a redução exponencial da fluência ao atravessar o paciente, calculada por ray-tracing voxel a voxel
Convolução com linhas de cone colapsado
A dose foi calculada pela convolução da TERMA com um kernel polienergético, aproximado por dezenas de linhas de cones colapsados. Cho implementou tipicamente 26 a 48 direções discretas. Em cada direção, a deposição de energia segue a formulação recursiva descrita na seção sobre Ahnesjö, com scaling por densidade voxel a voxel.
Validação contra dosimetria de filme
A validação experimental de Cho é particularmente relevante porque usa dosimetria de filme em condições realistas:
- PDDs (Percentage Depth Dose): calculados e medidos para campos de 5×5 a 20×20 cm² em energias de 6 e 15 MV
- Perfis laterais: em múltiplas profundidades, verificando penumbra, uniformidade e dose fora do campo
- Comparação com pencil beam: o CCC foi comparado também com um algoritmo pencil beam implementado no mesmo sistema
Os resultados mostraram concordância dentro de 2% entre CCC e medidas de filme para a grande maioria dos pontos, com exceção da região de build-up. Nessa região (primeiros milímetros), a modelagem empírica da contaminação eletrônica e a transição para equilíbrio eletrônico são difíceis de capturar analiticamente, resultando em discrepâncias maiores. Cho observou que o CCC apresentou desempenho significativamente superior ao pencil beam em situações com heterogeneidades, confirmando a vantagem teórica prevista por Ahnesjö.
Implementações Comerciais em TPS
O CCC foi adotado por diversos fabricantes de sistemas de planejamento de tratamento (TPS). Cada implementação tem particularidades, mas todas seguem o framework estabelecido por Mackie, Ahnesjö e validado por Cho:
Philips Pinnacle³
O Pinnacle foi o primeiro TPS comercial a implementar o CCC como algoritmo principal de cálculo de dose. Desenvolvido a partir dos trabalhos originais de Mackie et al. na Universidade de Wisconsin, o Pinnacle usa kernels de Mackie com a formulação de cone colapsado de Ahnesjö. Historicamente considerado o “padrão ouro” entre os algoritmos de convolução/superposição, o Pinnacle usa tipicamente 26 a 80 direções de cone, com opção de aumentar para geometrias complexas.
Elekta Oncentra (ex-Helax-TMS)
O Oncentra Masterplan tem conexão direta com Ahnesjö, que participou do desenvolvimento do Helax-TMS na Suécia. A implementação segue fielmente o artigo original de 1989. Quando a Elekta adquiriu a nucletron e depois integrou o Helax, o CCC do Oncentra foi mantido como um dos algoritmos de referência.
RayStation (RaySearch Laboratories)
O RayStation oferece tanto CCC quanto Monte Carlo. O CCC do RayStation é uma implementação moderna que aproveita paralelização em múltiplos cores e otimizações algorítmicas para atingir tempos de cálculo de segundos em grids típicos. É frequentemente usado como algoritmo de cálculo rápido durante a otimização inversa de IMRT/VMAT, com verificação final por Monte Carlo.
XiO e Monaco (Elekta)
O XiO (originalmente CMS Focus) utilizou CCC como algoritmo principal durante muitos anos. O Monaco, sucessor do XiO, migrou para Monte Carlo baseado em GPU como algoritmo primário, mas ainda utiliza princípios de convolução/superposição em módulos específicos.
ISOgray (DOSIsoft)
O ISOgray implementa CCC com formulação próxima à original de Ahnesjö, sendo amplamente utilizado na Europa, especialmente na França e nos países francófonos.
Contaminação eletrônica e dose de saída
A convolução de kernels pontuais abrange todos os voxels do volume do paciente, permitindo modelar obliquidade de superfície. Porém, a contaminação eletrônica proveniente do cabeçote e do ar não é capturada pelos kernels. Isso é tratado por uma componente empírica adicional, dependente de SSD, tamanho de campo e distância off-axis, que decresce exponencialmente desde a superfície até o alcance máximo dos elétrons contaminantes. Na saída do paciente, como não há contribuição de kernel do ar, há uma ligeira superestimação da dose — um efeito menor na maioria dos casos clínicos.
Tabela Comparativa: CCC vs Pencil Beam vs AAA vs Monte Carlo
A tabela abaixo compara os principais algoritmos de cálculo de dose para fótons disponíveis em sistemas de planejamento comerciais. A inclusão do AAA (Analytical Anisotropic Algorithm) da Varian e do Acuros XB complementa a comparação com algoritmos amplamente utilizados na prática clínica.
| Característica | Pencil Beam | CCC / Superposição | AAA (Varian) | Acuros XB | Monte Carlo |
|---|---|---|---|---|---|
| Base teórica | Convolução 2D com kernels invariantes | Superposição 3D com cones colapsados | Superposição com kernels anisotrópicos separados | Equação de transporte de Boltzmann (LBTE) | Simulação estocástica partícula por partícula |
| Ordem de cálculo | $n^3$ (conv. 2D) | $n^4 \times m$ | $n^4 \times m’$ | Determinístico, proporcional a $n^3$ | Estocástico ($N_{hist}$ partículas) |
| Heterogeneidades | Correção tipo-a (escala profundidade) | Scaling por densidade em 3D | Scaling por densidade com kernels separados | Transporte explícito em multi-material | Transporte explícito, exato |
| Transporte eletrônico lateral | Não modela | Aproximado (scaling retilíneo) | Aproximado (melhor que PB) | Sim (resolução determinística) | Sim (completo) |
| Penumbra em pulmão | Subestima alargamento | Razoável (±3-5%) | Razoável (±2-4%) | Precisa (±1-2%) | Exata (referência) |
| Dose em interface ar-tecido | Imprecisa | Boa para maioria dos casos | Boa para maioria dos casos | Precisa | Exata |
| Build-up | Empírico | Empírico (±2-5%) | Empírico (±2-5%) | Melhor (±1-3%) | Exato |
| Velocidade típica | Segundos | Segundos a minutos | Segundos a minutos | Minutos | Minutos a horas |
| GPU / paralelização | Não necessário | Suportado (RayStation, Monaco) | Suportado (Eclipse) | Sim (Eclipse) | Essencial (Monaco, RayStation) |
| TPS comerciais | Eclipse (PBC, descontinuado) | Pinnacle, Oncentra, RayStation, XiO | Eclipse (Varian) | Eclipse (Varian) | Monaco, RayStation, PRIMO |
*Acuros XB usa o método de transporte determinístico LBTE (Linear Boltzmann Transport Equation), não Monte Carlo puro, mas atinge precisão comparável na maioria dos cenários clínicos. Para aprofundamento sobre Monte Carlo, veja nosso guia sobre Monte Carlo em radioterapia e o artigo sobre aplicações de Monte Carlo para fótons.
Limitações e Situações Críticas do CCC
Apesar de sua robustez, o CCC apresenta limitações conhecidas que o físico médico deve considerar:
Falta de equilíbrio eletrônico em pulmão
Em feixes de alta energia (15-18 MV) atravessando pulmão, o CCC subestima o alargamento lateral da penumbra. Arnfield et al. (2000) demonstraram discrepâncias de 3-5% em regiões onde falta equilíbrio de partículas carregadas (CPE). A razão é que o scaling retilíneo do kernel assume que os elétrons secundários seguem trajetórias retas escaladas pela densidade — mas na realidade, em tecido de baixa densidade, os elétrons sofrem espalhamento múltiplo e percorrem caminhos mais tortuosos do que o modelo prevê. Esse efeito é mais pronunciado para campos pequenos em alta energia.
Região de build-up
Cho et al. (2012) documentaram discrepâncias maiores que 2% na região de build-up. A modelagem da contaminação eletrônica é empírica e a transição para equilíbrio eletrônico é difícil de capturar com a formulação analítica dos kernels. Na prática clínica, a dose no build-up raramente é o parâmetro dosimétrico determinante — mas em tratamentos superficiais ou com bolus, essa limitação pode ser relevante.
Interfaces de alta densidade
Em interfaces com materiais de alta densidade (próteses metálicas, implantes dentários, clips cirúrgicos), o CCC pode apresentar artefatos de dose nas primeiras camadas de tecido após o material denso. O scaling por densidade funciona razoavelmente para tecidos biológicos ($\rho$ de 0,001 a 1,85 g/cm³), mas os coeficientes de atenuação de metais diferem significativamente dos de água, e a composição atômica altera o espectro de partículas secundárias.
Discretização angular
O número de direções de cone ($m$) afeta tanto a precisão quanto o tempo de cálculo. Com apenas 26 direções, artefatos de “ray effect” podem aparecer em regiões distantes do isocentro. Implementações modernas usam 48 a 80 direções para minimizar esses artefatos, ao custo de maior tempo de cálculo. A escolha do número de direções é um compromisso entre resolução angular e velocidade.
Considerações Finais
O Collapsed Cone Convolution equilibra precisão e eficiência de uma forma que poucos algoritmos conseguem. Três décadas de literatura científica e prática clínica sustentam sua posição como um dos algoritmos mais utilizados em radioterapia.
Os kernels de deposição gerados por Monte Carlo (Mackie 1988) fornecem a base física — sem esses dados cuidadosamente simulados em geometria esférica com o código EGS, nenhum algoritmo de convolução seria possível. A formulação analítica polienergética e a aproximação de cones colapsados (Ahnesjö 1989) transformaram o conceito teórico em algoritmo computacionalmente viável, reduzindo a complexidade de $n^6$ para $n^4 \times m$ e demonstrando concordância com EGS4 em geometrias heterogêneas de 4 a 24 MeV. E as implementações práticas com modelos de múltiplas fontes (Cho 2012) demonstram que o CCC, quando corretamente comissionado com TERMA realista incluindo efeito horn, amolecimento e transmissão MLC, concorda com medidas de filme dentro de 2% para a maioria dos cenários clínicos.
Para cenários desafiadores — pulmão com feixes de alta energia, interfaces ar-tecido, campos pequenos sem equilíbrio eletrônico — o físico médico deve estar ciente das limitações do CCC e considerar algoritmos mais sofisticados como Monte Carlo ou Acuros XB. Mas para o dia a dia da radioterapia, desde 3D-CRT até IMRT e VMAT, o CCC permanece como uma das escolhas mais robustas disponíveis.
O conceito de superposição e TERMA é fundamental para entender como o CCC opera — a TERMA fornece a distribuição de energia total liberada, e o kernel descreve como essa energia se redistribui no meio. Para uma visão abrangente de todos os algoritmos disponíveis, consulte nosso hub sobre algoritmos de cálculo de dose por fótons.
Referências Principais
- Mackie TR, Scrimger JW, Battista JJ. A convolution method of calculating dose for 15-MV x rays. Med Phys. 1985;12(2):188-196.
- Mackie TR, Bielajew AF, Rogers DWO, Battista JJ. Generation of photon energy deposition kernels using the EGS Monte Carlo code. Phys Med Biol. 1988;33(1):1-20.
- Ahnesjö A. Collapsed cone convolution of radiant energy for photon dose calculation in heterogeneous media. Med Phys. 1989;16(4):577-592.
- Ahnesjö A, Aspradakis MM. Dose calculations for external photon beams in radiotherapy. Phys Med Biol. 1999;44(11):R99-R155.
- Cho W, Chung K, et al. Practical implementation of a collapsed cone convolution algorithm for a radiation treatment planning system. J Korean Phys Soc. 2012;61(12):2073-2083.
- Arnfield MR, Siantar CH, Siebers J, et al. The impact of electron transport on the accuracy of computed dose. Med Phys. 2000;27(6):1266-1274.