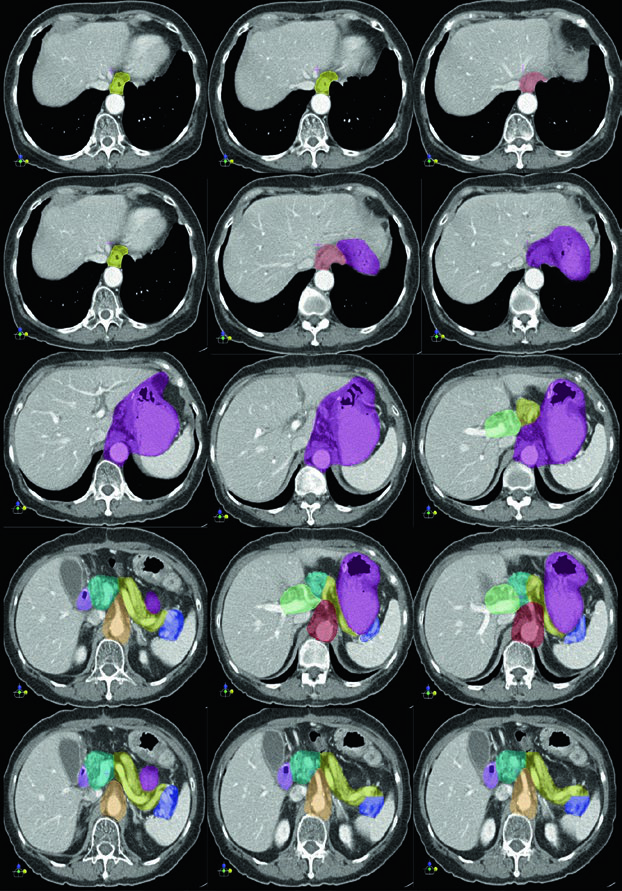
No câncer gástrico adjuvante, o contorno não nasce de uma lista fixa de linfonodos. Ele depende do subsite primário, do padrão de disseminação nodal e do tipo de gastrectomia realizada. É isso que organiza o CTV e explica por que diferentes cenários do mesmo órgão exigem desenhos distintos.
O texto fica muito mais humano quando assume essa lógica anatômica e deixa de soar como tradução expandida de tabelas.
Subsite e cirurgia definem o problema
Cardia, corpo, antro e piloro não puxam o mesmo raciocínio de drenagem. O mesmo vale para gastrectomia total e distal. O artigo original tem valor quando mostra que essas diferenças não são detalhes, mas a própria base do planejamento adjuvante.
É por isso que um bom texto precisa explicar o “porquê” antes de empilhar volumes sugeridos.
Rim, fígado e medula entram cedo na conversa
No câncer gástrico, não faz sentido desenhar o CTV e só depois pensar em órgãos em risco. A proximidade com rins, fígado e medula espinhal já molda a estratégia desde o início. Quando o artigo deixa isso claro, ele ganha maturidade clínica e foge do tom de conteúdo em série.
É esse tipo de integração que dá mais cara de autoria real ao texto.
T e N mudam a extensão do campo
Outro ponto importante é o impacto da categoria T e N na inclusão de estações linfonodais e no desenho do volume. Essa variação não deveria ser resumida como “mais estágio, mais campo”. O valor está em mostrar como o risco regional reconfigura o alvo de forma anatomicamente coerente.
Quando essa lógica aparece, o leitor percebe melhor a utilidade clínica do material.
Como a RT Medical Systems enxerga isso
- No câncer gástrico, subsite primário e cirurgia definem grande parte do contorno adjuvante.
- Órgãos em risco precisam ser considerados desde o início, não ao final do plano.
- T e N mudam a extensão do campo de forma anatômica, e isso precisa aparecer no texto.
O que muda na prática
- Subsite e tipo de gastrectomia devem estar explícitos antes da definição do CTV.
- Rins, fígado e medula devem entrar cedo na estratégia de planejamento.
- Exemplos por cárdia, corpo e antro/píloro ajudam mais quando acompanhados da lógica nodal.
Reescrever esse artigo em linguagem menos automática ajuda a mostrar que câncer gástrico em radioterapia não é um bloco único. O alvo muda porque a anatomia e a cirurgia mudam. Quando o texto assume isso, ele fica mais humano, mais claro e mais defensável.
Se sua equipe está revisando planejamento adjuvante no câncer gástrico, fale com nossos especialistas.
Transparência editorial
Revisão editorial: Equipe RT Medical Systems
Fonte editorial: capítulo clínico do artigo original e Target Volume Delineation and Field Setup
Atualizado em: 26/03/2026
- Reescrita integral com foco em subsite, cirurgia e lógica nodal.
- Redução do formato excessivamente tabelado do texto anterior.
- Ênfase em órgãos em risco e contexto anatômico.