Deep learning entra na linha de frente da imagem médica
A radiologia entrou em uma fase em que a qualidade de imagem deixou de ser apenas critério estético: ela é hoje variável crítica para detecção precoce de doenças e gestão do fluxo dentro do departamento. Marc Schaepkens, diretor de tecnologia da área de Imaging da GE HealthCare, descreveu em artigo recente publicado pela DOTmed como o deep learning está redefinindo o que é possível em tomografia computadorizada, ressonância magnética, PET/CT e raio-X — uma transição que combina redes neurais treinadas em grandes volumes de dados com hardware tradicional para resolver compromissos antigos da prática clínica.

Segundo Schaepkens, mais de 80% dos atendimentos em saúde envolvem algum exame de imagem. Esse volume crescente, somado à pressão por diagnósticos mais rápidos e precisos, expôs limitações dos algoritmos clássicos de reconstrução. O deep learning entra como subdomínio da inteligência artificial que aprende padrões a partir de grandes conjuntos de exames anteriores e otimiza a saída para preservar detalhes anatômicos sutis — desde um nódulo pulmonar pequeno até alterações intersticiais iniciais.
O que muda em CT, RM, PET e raio-X
Em tomografia computadorizada, a reconstrução tradicional sempre exigiu equilibrar quatro variáveis: ruído, resolução, velocidade de aquisição e dose de radiação. Modelos de deep learning conseguem entregar imagens com melhor relação sinal-ruído sem aumentar a dose, preservando a textura natural — fator importante para o radiologista habituado à estética das imagens convencionais. Estudos comparativos têm mostrado ganho consistente em detectabilidade de baixo contraste e redução de ruído frente a técnicas iterativas.
Em ressonância magnética, o ganho mais visível está na aceleração de aquisição. Trabalhos validados mostram redução significativa do tempo de exame mantendo a integridade diagnóstica. Para clínicas com agenda apertada, isso se traduz em mais pacientes atendidos por dia e menos artefatos de movimento, especialmente em populações pediátricas e idosos com dificuldade de manter imobilidade.
Em medicina nuclear e PET/CT, redes profundas têm melhorado tanto a qualidade visual quanto a precisão quantitativa, com impacto direto em oncologia: avaliação de resposta ao tratamento e monitoramento de lesões pequenas dependem dessa precisão. No raio-X, a aplicação mais consistente é o processamento de imagem com IA para padronizar a visualização de estruturas anatômicas-chave entre operadores e equipamentos diferentes.
Como a reconstrução com IA é incorporada ao pipeline
Reconstrução baseada em deep learning não substitui o pipeline tradicional; ela é incorporada em pontos específicos do processo, geralmente após a aquisição bruta dos dados (raw data) e antes da apresentação ao radiologista. A rede aprende a remover ruído, recuperar resolução espacial e suavizar artefatos sem introduzir alucinações — risco que motivou debates intensos na comunidade nos últimos cinco anos.
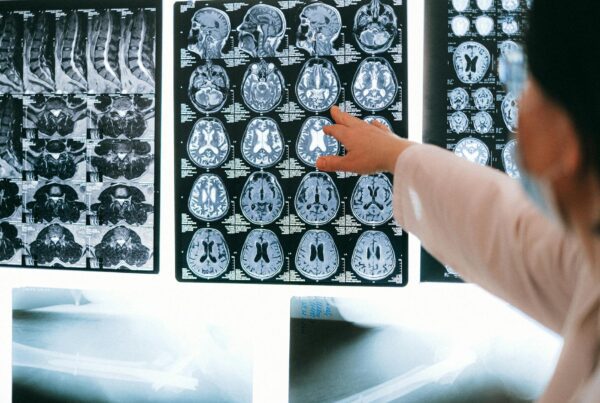
Estudos publicados em revistas como Radiology e European Radiology mostraram que algoritmos de reconstrução com deep learning oferecem ganhos consistentes em detectabilidade de baixo contraste em TC, particularmente importantes para identificar lesões hepáticas, pancreáticas e nódulos pulmonares pequenos. A IA tem superado radiologistas em detecção precoce de câncer pancreático, segundo trabalhos recentes que reforçam o caminho.
A GE HealthCare também enfatiza que esses avanços precisam ser acompanhados de validação clínica robusta. Casos de viés algorítmico, generalização entre populações e robustez frente a artefatos de aquisição precisam ser endereçados antes de adoção em massa — ponto reforçado por reguladores como FDA e ANVISA, que exigem evidência multicêntrica antes de autorizar uso clínico.
Implicações para a prática clínica
Para o radiologista no dia a dia, o impacto mais imediato é a redução do tempo de leitura quando a qualidade da imagem é mais consistente. Detectar um nódulo pulmonar de 4 mm ou doença intersticial inicial deixa de exigir múltiplas reformatações ou janelas customizadas. Como vendors integram IA em plataformas únicas, a tendência é que esses ganhos cheguem ao fluxo via PACS sem etapas adicionais.
Departamentos podem aumentar o throughput sem comprometer qualidade — algo que dialoga diretamente com a escassez global de radiologistas. O deep learning não substitui o profissional; libera tempo para casos complexos, segunda opinião e supervisão de fluxos automatizados. Para o Brasil, onde a relação radiologista por habitante ainda é desigual entre regiões, essas ferramentas têm potencial real de redistribuir capacidade técnica entre centros menores e hospitais de referência.
Perspectivas e próximos passos
O próximo passo apontado por Schaepkens é unir reconstrução com IA a fluxos de detecção e priorização automatizadas. Vendors estão explorando arquiteturas em que o deep learning não atua apenas no "como" reconstruir, mas no "o que" reportar primeiro — auxiliando triagem em departamentos sobrecarregados.
Limitações importantes permanecem: necessidade de bases de treinamento diversas, transparência sobre falhas dos modelos e protocolos para auditoria contínua. O fluxo expressivo de capital para empresas de IA radiológica sinaliza que o setor leva a sério essa convergência. A tendência é clara: deep learning deixa de ser feature opcional e passa a ser camada estrutural da imagem médica moderna.
Fonte: DOTmed — A new era of clarity, por Marc Schaepkens (GE HealthCare)