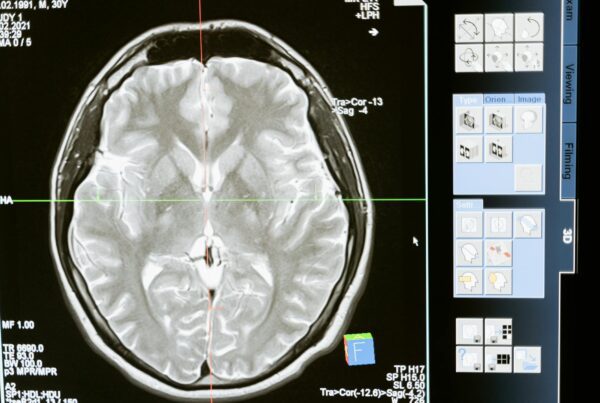
O que um nomograma de TC pode entregar
Pesquisadores apresentaram, em publicação recente noticiada pela AuntMinnie, um nomograma baseado em tomografia computadorizada (TC) que se propõe a apoiar decisões clínicas no câncer de ovário avançado. A proposta segue uma tendência consolidada na literatura: combinar achados de imagem com variáveis clínicas em uma calculadora visual, capaz de estimar probabilidades como ressecção cirúrgica completa, resposta à quimioterapia neoadjuvante ou recidiva precoce.
Por que essa decisão é tão difícil sem ferramentas objetivas
O câncer de ovário avançado, geralmente diagnosticado em estágios FIGO III ou IV, é tratado com duas estratégias complementares: cirurgia citorredutora primária seguida de quimioterapia ou quimioterapia neoadjuvante (NACT) seguida de cirurgia citorredutora intervalar (IDS). A escolha entre essas vias depende, sobretudo, da chance de obter citorredução completa (R0) ou ótima (resíduo < 1 cm). Ressecção incompleta está consistentemente associada a piores desfechos oncológicos.
Na prática clínica, a estimativa pré-operatória dessa chance ainda é heterogênea. Critérios de exame físico, marcadores tumorais como o CA-125, achados de TC e até laparoscopia diagnóstica são combinados de forma muitas vezes informal. Escores de imagem como o índice de carcinomatose peritoneal (PCI) e o escore de Suidan tentam padronizar a avaliação, mas ainda há variabilidade interobservador relevante.
O conceito por trás de um nomograma de TC
Um nomograma é uma representação gráfica de um modelo de regressão multivariada. O leitor traça uma reta sobre os pontos atribuídos a cada variável, soma os escores parciais e obtém uma probabilidade individualizada do desfecho. Essa abordagem é apreciada na prática por três motivos: traduz um modelo estatístico em um instrumento de cabeceira, explicita o peso relativo de cada variável e pode ser calibrada para diferentes populações.
Em câncer de ovário, nomogramas baseados em TC tipicamente combinam variáveis clínicas (idade, ECOG, CA-125, estado nutricional) com variáveis de imagem (volume de ascite, comprometimento omental, infiltração mesentérica, linfonodos suprarrenais, doença diafragmática, envolvimento intestinal). Em estudos recentes, modelos derivados de radiomics — quantificando textura, intensidade e morfologia de lesões — também passaram a alimentar essas calculadoras, ampliando o poder discriminativo em comparação com leituras puramente visuais.
Como esse tipo de ferramenta entra no consultório
Imagine uma paciente com massa pélvica volumosa, ascite e implantes peritoneais difusos vistos em TC. Em vez de discutir cirurgia primária com base apenas em impressão clínica, a equipe pode consultar o nomograma, inserir variáveis padronizadas e obter, por exemplo, uma probabilidade de citorredução completa de 30%. Esse número orienta a discussão multidisciplinar entre ginecologia oncológica, oncologia clínica e radiologia, e ajuda a definir se o caminho mais racional é NACT antes da cirurgia ou cirurgia primária em centro de referência.
O ganho não é apenas tecnológico. É também de governança clínica. Ao registrar a estimativa do nomograma no prontuário, a equipe documenta a justificativa para o plano terapêutico e cria base para auditoria de qualidade. Esse uso conversa diretamente com o avanço de relatórios estruturados em radiologia oncológica e com a discussão sobre eficiência de interpretação radiológica.
Variáveis de imagem que costumam pesar no modelo
Embora cada nomograma tenha sua composição própria, alguns achados de TC aparecem com frequência alta nos modelos publicados. Carcinomatose difusa do mesentério da raiz do intestino delgado costuma ser preditor forte de citorredução incompleta, assim como doença na cápsula hepática profunda, na fissura de Glisson e em pedículos vasculares centrais. A presença de linfonodos suprarrenais e cardiofrênicos também eleva a complexidade cirúrgica. Por outro lado, ascite isolada, doença omental e implantes pélvicos com bordas bem definidas costumam estar associados a maior chance de ressecção completa.
Esses achados não falam por si: a interpretação depende de protocolo padronizado, com TC multifase de abdome e pelve com contraste iodado, cortes finos e reformatações coronal e sagital. Em centros que adotam IA na quantificação de carga tumoral peritoneal, a saída do algoritmo pode ser usada como insumo do nomograma, num pipeline parecido com o que aparece em aplicações de IA para análise quantitativa de imagem.
Limitações que precisam estar no radar
Como toda ferramenta de predição, nomogramas têm pontos cegos. Validação externa em populações diferentes é fundamental: um modelo desenvolvido em centro acadêmico de alto volume pode não se traduzir bem em hospital regional. A heterogeneidade dos critérios de citorredução completa entre cirurgiões também afeta a calibração: o que um time considera “R0” pode ser “resíduo mínimo” em outro. Por fim, há viés de seleção quando o modelo é treinado em pacientes que de fato chegaram à cirurgia, deixando de fora aqueles considerados inoperáveis logo no exame inicial.
Outra limitação relevante diz respeito ao impacto clínico real. Um modelo pode ter alta acurácia estatística e, ainda assim, não modificar desfechos se não estiver integrado ao processo decisório. Por isso, ferramentas como essa só agregam valor quando incorporadas a discussões multidisciplinares formais e a protocolos institucionais.
Por que isso importa no Brasil
O câncer de ovário tem incidência crescente em mulheres adultas no Brasil e mortalidade alta, em parte porque o diagnóstico costuma ser tardio. Centros de referência em oncologia ginecológica já discutem caso a caso o melhor caminho terapêutico, mas a maioria das pacientes ainda é tratada em hospitais sem expertise específica em cirurgia oncológica complexa. Nomogramas de TC podem ajudar tanto na decisão clínica quanto na referenciação adequada para centros de alto volume — um dos fatores mais consistentemente associados a melhores desfechos.
A adoção brasileira passa por três barreiras práticas: padronização de protocolos de TC, capacitação na leitura sistemática de carcinomatose peritoneal e implantação de fluxos digitais que permitam registrar e auditar as estimativas. Centros que avançarem nessas frentes terão vantagem competitiva e clínica no manejo do câncer ginecológico avançado.
Perspectivas: TC, radiomics e modelos multimodais
O caminho natural é integrar nomogramas de TC com modelos multimodais que incluam dados moleculares (mutação BRCA, status HRD), evolução de marcadores tumorais e até features de ressonância magnética para casos selecionados. Modelos de IA capazes de processar a TC inteira, em vez de medidas pontuais, devem aumentar a robustez do escore. Em paralelo, ensaios prospectivos precisam mostrar não só capacidade preditiva, mas também impacto em sobrevida global e em qualidade de vida.
O ponto a guardar deste anúncio é prático: a ferramenta certa, no momento certo da decisão, pode mudar trajetórias terapêuticas inteiras. Para a radiologia, é também uma confirmação de que o radiologista está cada vez mais inserido no centro do plano oncológico, não apenas na descrição dos achados.
Fonte: AuntMinnie