La delineación del volumen blanco en cáncer gástrico depende del subsite primario, del patrón de diseminación ganglionar y del tipo de gastrectomía realizada. El capítulo mantiene toda la discusión en el escenario adyuvante posoperatorio y define con claridad qué entra en el CTV, cuándo el ahorro renal modifica el campo y cómo revisar el plan sin perder de vista médula, riñones e hígado.
Para una visión más amplia del tema, revise el Target Volume Delineation and Field Setup – Complete Clinical Guide. Si quiere comparar cómo cambia la lógica nodal en otra localización anatómica, también puede ver nuestro artículo sobre carcinoma de orofaringe.
En este artículo
- Anatomía y patrones de diseminación
- Estudio diagnóstico relevante para la delineación
- Principios generales de planificación y delineación del volumen blanco
- CTV para adenocarcinoma de cardias tras gastrectomía total
- CTV para adenocarcinoma del cuerpo gástrico tras gastrectomía distal
- CTV para adenocarcinoma de antro o píloro tras gastrectomía distal
- Evaluación del plan
Anatomía y Patrones de Diseminación
En cáncer gástrico, el diseño del campo empieza con una realidad muy concreta: cardias, cuerpo y estómago distal no fallan igual. El estómago va desde la unión gastroesofágica hasta el píloro, se divide en cardias, fundus, cuerpo y antro, y su pared se organiza en mucosa, submucosa, muscular propia, subserosa y serosa.
El capítulo subraya la relación inmediata con lóbulo hepático izquierdo, bazo, glándula suprarrenal izquierda, polo superior del riñón izquierdo, páncreas, colon transverso y grandes vasos alrededor del tronco celíaco y la arteria mesentérica superior. Esa vecindad explica por qué la extensión local puede alcanzar hígado, duodeno, páncreas, colon transverso, epiplón y diafragma, mientras que los tumores proximales pueden ascender hacia el esófago. También puede existir invasión perineural.
La distribución por localización primaria tampoco es homogénea: cerca del 35% aparece en unión gastroesofágica, cardias o fundus, alrededor del 25% en el cuerpo y aproximadamente el 40% en antro o estómago distal. La afectación ganglionar regional está presente en hasta el 80% de los casos al diagnóstico. Los tumores proximales pueden extenderse a ganglios paraesofágicos bajos, los del cuerpo pueden comprometer todos los territorios ganglionares y las lesiones distales del antro pueden alcanzar cadenas periduodenales y del hilio hepático.
Lymph node stations commonly involved in gastric cancer
This table organizes the JRSGC nodal stations cited in the chapter and helps align each subsite with its expected drainage pattern.
| Category | Station | Description |
|---|---|---|
| N1 | 1 | Right cardial nodes |
| N1 | 2 | Left cardial nodes |
| N1 | 3 | Nodes along lesser curvature |
| N1 | 4 | Nodes along greater curvature |
| N1 | 5 | Suprapyloric nodes |
| N1 | 6 | Infrapyloric nodes |
| N2 | 7 | Nodes along left gastric artery |
| N2 | 8 | Nodes along common hepatic artery |
| N2 | 9 | Nodes along celiac axis |
| N2 | 10 | Nodes at the splenic hilus |
| N2 | 11 | Nodes along splenic artery |
| N3 | 12 | Nodes in the hepatoduodenal ligament |
| N3 | 13 | Nodes at the posterior aspect of pancreatic head |
| N3 | 14 | Nodes at the root of mesenterium |
| N4 | 15 | Nodes in the mesocolon of transverse colon |
| N4 | 16 | Para-aortic lymph nodes |
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.1). Figure and table adapted from Hartgrink, Van De Velde (2005) Status of extended lymph node dissection: Journal of Surg Oncol 90:153-165. Used with permission from Wiley Inc.
Estudio Diagnóstico Relevante para la Delineación
Antes de contornear, el capítulo exige revisar el informe quirúrgico, el informe anatomopatológico y discutir el caso con el cirujano. La razón es práctica: la zona de mayor riesgo de recidiva no siempre se reconoce solo en la tomografía posoperatoria, y la diferencia entre gastrectomía total y parcial cambia lo que debe incluirse.
La tomografía preoperatoria debe releerse para identificar la localización original del tumor y las cadenas ganglionares regionales afectadas. El texto también es explícito con el PET con 18-FDG: por sí solo no es un método suficiente para el estadiaje preoperatorio del cáncer gástrico, porque los subtipos difusos y mucinosos muestran baja captación. Cuando la función renal puede limitar el tratamiento, se puede considerar un estudio cuantitativo de perfusión renal antes de radioterapia.
La tomografía diagnóstica posoperatoria con contraste oral e intravenoso debe identificar esófago y remanente gástrico, anastomosis gastro-yeyunal u esófago-yeyunal, muñón duodenal, porta hepatis, hilio esplénico, páncreas, arteria celíaca y arteria mesentérica superior. El capítulo cierra esta sección recordando que el tipo de cirugía depende de la localización tumoral y del patrón histológico.
Principios Generales de Planificación y Delineación del Volumen Blanco
La preparación adyuvante comienza con ayuno de 2 a 3 horas antes de la simulación y antes de cada sesión. La tomografía de planificación debe tener cortes de 3 a 5 mm, con el paciente en decúbito supino y brazos elevados, cubriendo desde el domo diafragmático, o desde la carina cuando el tumor compromete unión gastroesofágica o cardias, hasta el borde inferior de L4.
Para IMRT, se recomienda inmovilización con bolsa de vacío tipo VacLok. El contraste intravenoso es preferible porque el capítulo utiliza los vasos como referencias de contorneo, sobre todo para la cobertura ganglionar. La tomografía preoperatoria debe permanecer disponible durante el delineado porque ayuda a reconstruir el volumen tumoral original y los grupos ganglionares que deben quedar dentro del campo adyuvante.
El capítulo identifica tres componentes que siempre deben reconocerse en el CTV adyuvante: lecho tumoral, anastomosis o muñones quirúrgicos y linfáticos regionales. Luego añade un detalle que cambia muchos planes: el ligamento hepatogástrico debería tratarse preferentemente en todos los casos, ya que contiene ganglios gástricos derechos e izquierdos que no siempre se resecan por completo.
Si se usa IMRT, deben delinearse tanto el lecho tumoral como las regiones linfáticas subclínicas. La expansión del PTV se basa en movimiento orgánico e incertidumbre de posicionamiento, con un mínimo sugerido de 1 cm. La dosis adyuvante recomendada con quimioterapia concomitante es 45 Gy en 25 fracciones con fotones de al menos 6 MV, y puede aumentarse a 50,4-54 Gy si existen márgenes positivos o enfermedad residual y la tolerancia de órganos críticos lo permite.
Target volume definition and description
The chapter separates gross disease, postoperative subclinical coverage, and boost logic. That distinction avoids mixing the adjuvant CTV with boost volumes for residual disease or positive margins.
| Target volumes | Definition and description |
|---|---|
| GTV | Gross residual disease defined by CT imaging and surgical findings. |
| PTV (residual disease) | GTV/positive margins + 1.5 cm. Cone down boost after 45 Gy to a total dose of 50.4-54 Gy in 1.8 Gy/fraction. |
| CTV45 | Coverage of nodal groups according to subsite (see Tables 15.5, 15.6, 15.7, and 15.8). Also includes remnant stomach, anastomosis (gastrojejunal, oesophagojejunal), duodenal stump. |
| PTV45 | CTV45 + 1 cm margin. A larger margin may be required for organ motion and setup uncertainties. |
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.2)
General considerations for clinical target volume
These points are the practical checks that change contour boundaries after partial or total gastrectomy.
| Target volumes | Definition and description |
|---|---|
| Duodenal stump | Should preferably be covered in patients who have had a partial gastrectomy for distal/antral tumours. Should not be covered in patients with proximal/cardia tumours who have had a total gastrectomy. |
| Anastomosis | Gastrojejunal anastomosis (partial gastrectomy for tumours of the distal stomach). Oesophagojejunal anastomosis (total gastrectomy for tumours of proximal stomach or GE junction) should be treated. |
| Para-aortic nodes | Should be included for the entire length of the CTV. |
| Paraoesophageal nodes | 4 cm margin of the oesophagus should be included in the clinical target volume for tumours of the gastro-esophageal junction. |
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.3)
Impact of T and N category on field inclusion
The chapter also condenses when remaining stomach, tumour bed, and nodal sites enter the field according to TN category.
| AJCC eighth edition TN category | Remaining stomach | Tumour bed | Nodes |
|---|---|---|---|
| T1-2N0 (not into subserosa) | No | No | No |
| T2N0 (into subserosa) | Variable | Yes | No |
| T3N0 | Variable | Yes | No |
| T4N0 | Variable | Yes | Variable |
| T1-2N+ | Yes | No | Yes |
| T3-4N+ | Yes | Yes | Yes |
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.4). This table was published in Clinical Radiation Oncology, fourth Edition, Leonard et al., page 928, Copyright Elsevier.
Recommended target volumes: gastro-esophageal junction
For GE junction disease, the field composition changes with depth of invasion, nodal positivity, and the ability to spare the right kidney.
| Site of primary and stage | Remaining stomacha | Tumour bed volumesa | Nodal volume |
|---|---|---|---|
| GE Junction | If allows exclusion of 2/3 right kidney | T stage dependent | N stage dependent |
| T2N0, invasion of subserosa | Variable, dependent on surgical pathological findingsb | Medial left hemidiaphragm; adjacent body of pancreas | None or PG, PEN |
| T3N0 | Variable, dependent on surgical pathological findingsb | Medial left hemidiaphragm; adjacent body of pancreas | None or PG, PEN, CN, MNc |
| T4N0 | Preferable but dependent on surgical pathological findingsb | As for T3N0 plus site(s) of adherence with 3-5 cm margin | Nodes related to site(s) of adherence +/- PG, PEN, CN, MN |
| T1-2N+ | Preferable | Not indicated for T1; as above for T2 into subserosa | PG, PEN, CN, MN |
| T3-4N+ | Preferable | As for T3N0, T4N0 | As for T1-2N+ and T4N0 |
Abbreviations: PG perigastric, CN celiac, PEN perioesophageal, MN mediastinal.
a Use preoperative imaging (CT, barium swallow), surgical clips, and post-operative imaging (CT, barium swallow). b For tumours with >5 cm margins confirmed pathologically, treatment of residual stomach is optional, especially if this would result in substantial increase in normal tissue morbidity. c Optional node inclusion for T2-3N0 lesions if adequate surgical node dissection (D2) and at least 10-15 nodes are examined pathologically.
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.5). This table was published in Clinical Radiation Oncology, fourth Edition, Leonard et al., page 928, Copyright Elsevier.
Recommended target volumes: cardia or proximal third of stomach
Cardia and proximal-third tumours keep the same stage logic, but the recommended nodal additions broaden once nodal disease is documented.
| Site of primary and stage | Remaining stomacha | Tumour bed volumesa | Nodal volume |
|---|---|---|---|
| Cardia/Proximal third of stomach | Yes, but spare 2/3 of one kidney, usually right | T category dependent | N category dependent |
| T2N0, invasion of subserosa | Variable, dependent on surgical pathological findingsb | Medial left hemidiaphragm, adjacent body of pancreas +/- tail | None or PGc |
| T3N0 | Variable, dependent on surgical pathological findingsb | Medial left hemidiaphragm, adjacent body of pancreas +/- tail | None or PG. Optional: PEN, CN, MNc |
| T4N0 | Variable, dependent on surgical pathological findingsb | As for T3N0 plus site(s) of adherence with 3-5 cm margin | Nodes related to site(s) of adherence +/- PG, CN, MN |
| T1-2N+ | Preferable | Not indicated for T1 | PG, CN, splenic, SP, +/- MN, PD, PHd |
| T3-4N+ | Preferable | As for T3N0, T4N0 | As for T1-2N+ and T4N0 |
Abbreviations: PG perigastric, CN celiac, SP suprapancreatic, PH porta hepatis, PD pancreaticoduodenal, PEN perioesophageal, MN mediastinal.
a Use preoperative imaging (CT, barium swallow), surgical clips, and post-operative imaging (CT, barium swallow). b For tumours with >5 cm margins confirmed pathologically, treatment of residual stomach is optional, especially if this would result in substantial increase in normal tissue morbidity. c Optional node inclusion for T2-3N0 lesions if adequate surgical node dissection (D2) and at least 10-15 nodes are examined pathologically. d Pancreaticoduodenal and porta hepatis nodes are at low risk if nodal positivity is minimal (1-2 positive nodes with 10-15 nodes examined), and this region does not need to be irradiated. Perioesophageal and mediastinal nodes are at risk if there is oesophageal extension.
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.6). This table was published in Clinical Radiation Oncology, fourth Edition, Leonard et al., page 928, Copyright Elsevier.
Recommended target volumes: body or middle third of stomach
For body lesions, the remnant stomach is consistently retained and the tumour bed tracks the pancreas, with optional nodal escalation when dissection is adequate.
| Site of primary and stage | Remaining stomacha | Tumour bed volumesa | Nodal volume |
|---|---|---|---|
| Body/mid third of stomach | Yes, but spare 2/3 of one kidney | T category dependent | N category dependent, spare 2/3 of one kidney |
| T2N0, invasion of subserosa | Yes | Body of pancreas +/- tail | None or PG. Optional: CN, splenic, SP, PD, PHb |
| T3N0 | Yes | Body of pancreas +/- tail | None or PG. Optional: CN, splenic, SP, PD, PHb |
| T4N0 | Yes | As for T3N0 plus site(s) of adherence with 3-5 cm margin | Nodes related to site(s) of adherence +/- PG, CN, splenic, SP, PD, PH |
| T1-2N+ | Yes | Not indicated for T1 | PG, CN, splenic, SP, PD, PH |
| T3-4N+ | Yes | As for T3N0, T4N0 | As for T1-2N+ and T4N0 |
Abbreviations: PG perigastric, CN celiac, SP suprapancreatic, PH porta hepatis, PD pancreaticoduodenal, PEN perioesophageal, MN mediastinal.
a Use preoperative imaging (CT, barium swallow), surgical clips, and post-operative imaging (CT, barium swallow). b Optional node inclusion for T2-3N0 lesions if adequate surgical node dissection (D2) and at least 10-15 nodes are examined pathologically.
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.7). This table was published in Clinical Radiation Oncology, fourth Edition, Leonard et al., page 929, Copyright Elsevier.
Recommended target volumes: antrum, pylorus, or distal third
Distal gastric primaries shift the tumour bed toward the pancreatic head and duodenum, and they are the cases in which the duodenal stump becomes most relevant.
| Site of primary and stage | Remaining stomacha | Tumour bed volumesa | Nodal volume |
|---|---|---|---|
| Pylorus/distal third of stomach | Yes, but spare 2/3 of one kidney, usually left | T category dependent | N category dependent, spare 2/3 of one kidney |
| T2N0, invasion of subserosa | Variable, dependent on surgical pathological findingsb | Head of pancreas +/- body, first and second portion of duodenum | None or PG. Optional: CN, SP, PD, PHc |
| T3N0 | Variable, dependent on surgical pathological findingsb | Head of pancreas +/- body, first and second portion of duodenum | None or PG. Optional: CN, SP, PD, PHc |
| T4N0 | Variable, dependent on surgical pathological findingsb | As for T3N0 plus site(s) of adherence with 3-5 cm margin | Nodes related to site(s) of adherence +/- PG, CN, SP, PD, PH |
| T1-2N+ | Preferable | Not indicated for T1 | PG, CN, SP, PD, PH. Optional: Splenic hilum |
| T3-4N+ | Preferable | As for T3N0, T4N0 | As for T1-2N+ and T4N0 |
Abbreviations: PG perigastric, CN celiac, SP suprapancreatic, PH porta hepatis, PD pancreaticoduodenal, PEN perioesophageal, MN mediastinal.
a Use preoperative imaging (CT, barium swallow), surgical clips, and post-operative imaging (CT, barium swallow). b For tumours with >5 cm margins confirmed pathologically, treatment of residual stomach is optional, especially if this would result in substantial increase in normal tissue morbidity. c Optional node inclusion for T2-3N0 lesions if adequate surgical node dissection (D2) and at least 10-15 nodes are examined pathologically.
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.8). This table was published in Clinical Radiation Oncology, fourth Edition, Leonard et al., page 929, Copyright Elsevier.
Volúmenes Clínicos Blanco para T1N1M0 de Cardias tras Gastrectomía Total
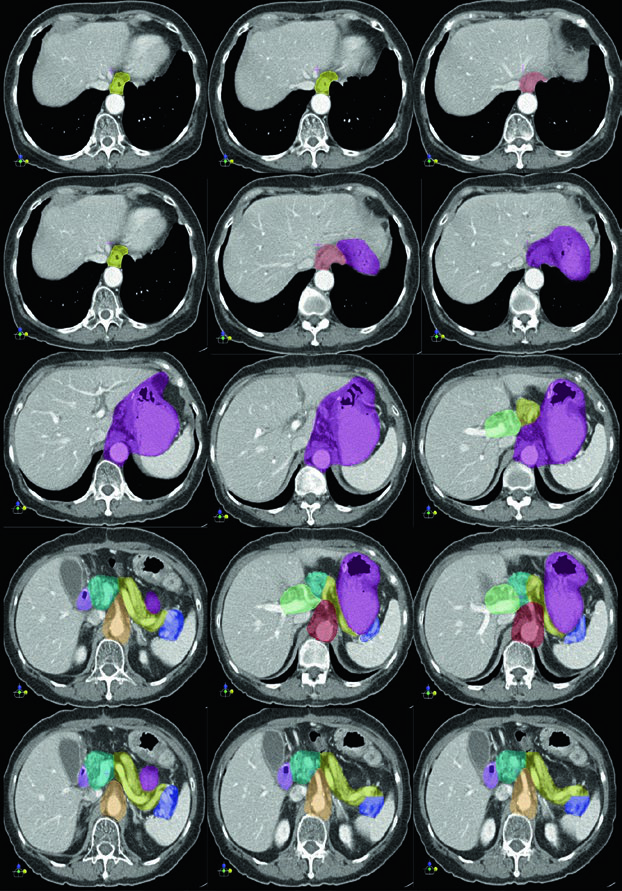
En este caso proximal, la cobertura esencial incluye la anastomosis esófago-yeyunal, el ligamento hepatogástrico, la arteria celíaca y el hilio esplénico. El capítulo usa este ejemplo para mostrar que la gastrectomía total no elimina las vías de riesgo proximal; simplemente desplaza el centro del campo hacia el esófago distal y el drenaje nodal central.
La secuencia axial sigue el contorno alrededor de la anastomosis y de los vasos centrales. Esa lógica visual coincide con las tablas para unión gastroesofágica y cardias, donde las cadenas paraesofágicas, celíacas y mediastínicas se amplían o se reducen según estadio T, extensión esofágica y estado ganglionar.
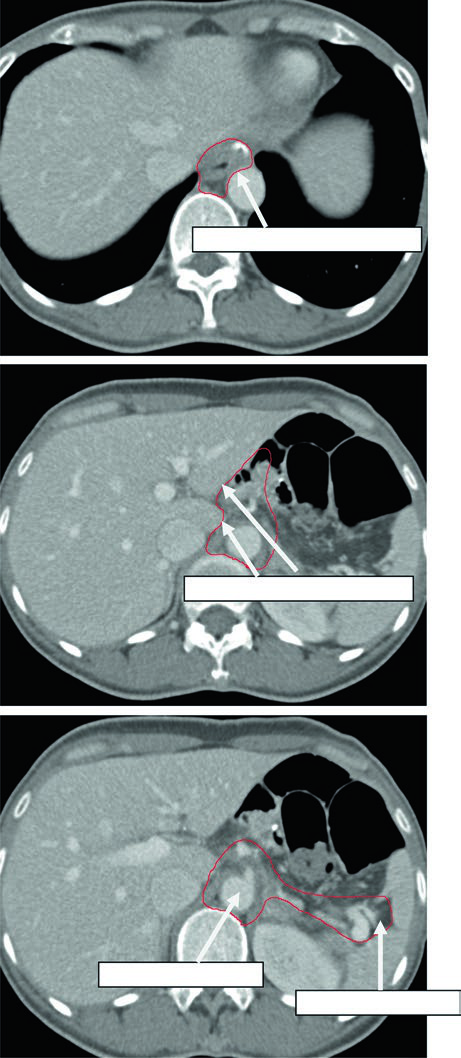
La enseñanza más útil aquí es quirúrgica. Cuando el estómago ya fue resecado, el remanente deja de ser problema, pero la anastomosis y las estaciones ganglionares de mayor riesgo siguen definiendo el núcleo del plan.
Volúmenes Clínicos Blanco para T3N3M0 del Cuerpo Gástrico tras Gastrectomía Distal
Para un primario del cuerpo gástrico tratado con gastrectomía distal, el capítulo muestra cobertura de la anastomosis gastro-yeyunal, del remanente gástrico, de la arteria celíaca y del hilio esplénico. Eso coincide con la regla general del texto: los tumores del cuerpo pueden comprometer todos los sitios ganglionares, y la positividad nodal refuerza la necesidad de cubrir drenaje central y esplénico.
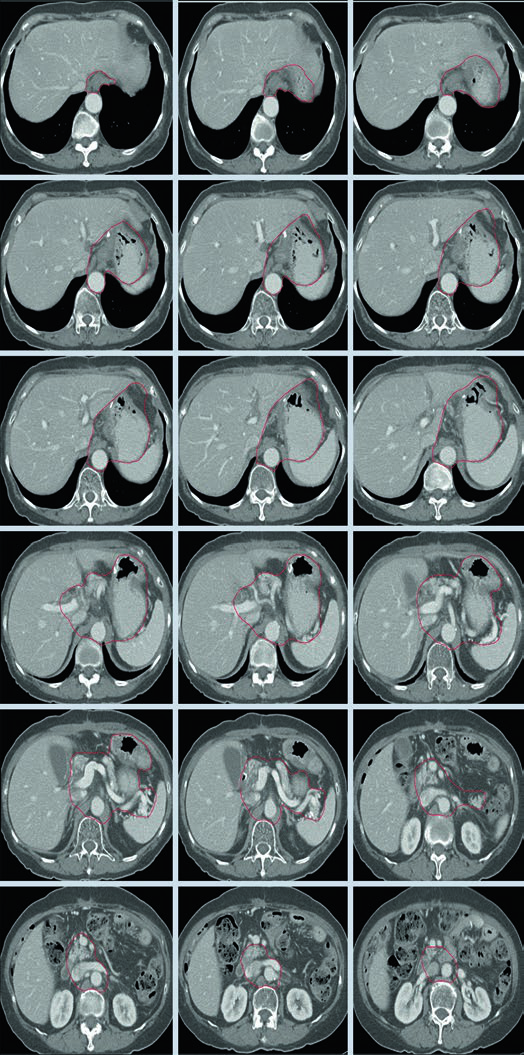
En este ejemplo, el remanente gástrico permanece dentro del volumen y el lecho tumoral sigue el cuerpo del páncreas, con o sin cola, tal como describe la tabla para lesiones del tercio medio. La imagen también deja claro que la arteria celíaca y el hilio esplénico no son añadidos decorativos; forman parte de la vía de drenaje esperada.
Volúmenes Clínicos Blanco para T2N1M0 de Antro o Píloro tras Gastrectomía Distal
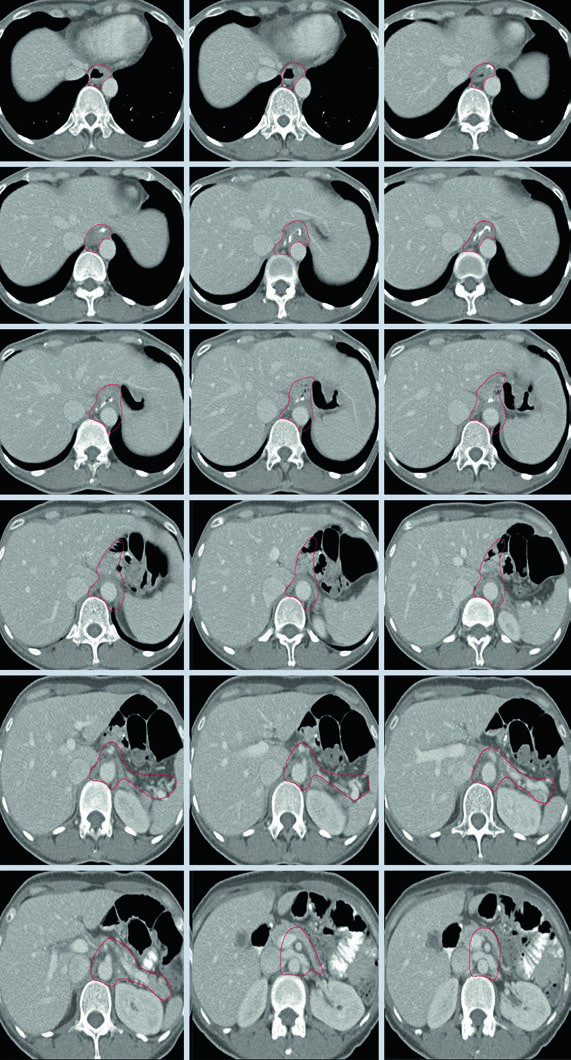
En la enfermedad distal cambia el énfasis. La anastomosis gastro-yeyunal sigue siendo importante, pero el capítulo añade remanente gástrico, ligamento hepatogástrico, muñón duodenal y, de forma opcional, hilio esplénico.
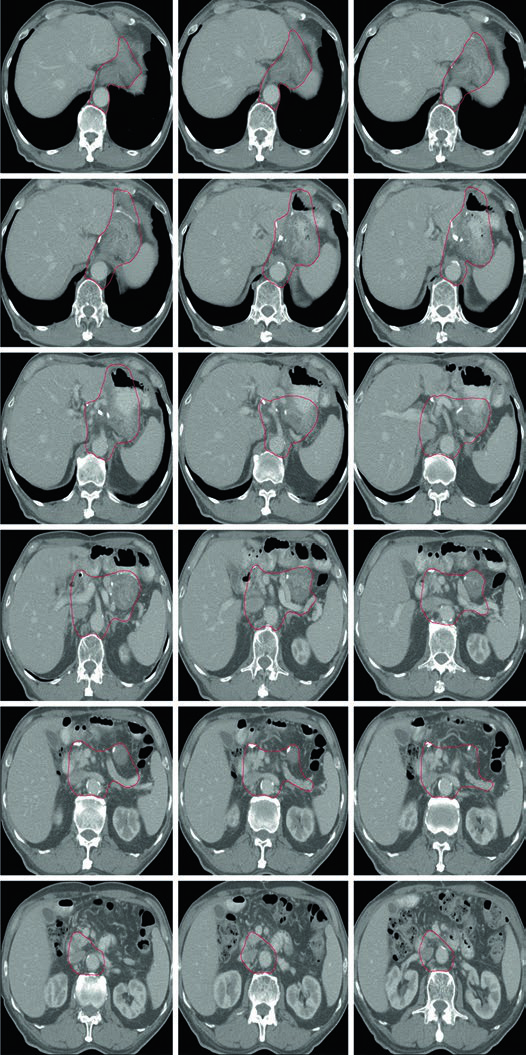
Ese patrón encaja con la vía de diseminación descrita al inicio: los tumores distales y del antro pueden comprometer cadenas periduodenales y porta hepatis. Cuando el capítulo insiste en el muñón duodenal y en el ligamento hepatogástrico, está conectando el contorneo posoperatorio con un riesgo locorregional documentado.
Evaluación del Plan
En casos avanzados, el capítulo prioriza de forma explícita las restricciones de tejido sano por encima de la cobertura completa del tumor, sobre todo para médula espinal, riñones e hígado. Es una regla muy práctica en abdomen superior y define cómo debe juzgarse un compromiso aceptable.
Con técnica conformada 3D, idealmente el 100% del PTV45 debe recibir al menos 42,75 Gy, es decir, el 95% de la prescripción, según ICRU 62. Con IMRT, la referencia pasa a 98% del PTV recibiendo al menos 42,75 Gy, de acuerdo con ICRU 83. Antes de aprobar el plan, el capítulo exige contornear de forma formal los órganos de riesgo alrededor del CTV.
Dose limitations of OAR in radiation therapy for upper abdominal malignancies
Plan assessment in this chapter is grounded in organ-at-risk tolerance, not only in target coverage. The table below condenses the quoted upper-abdominal constraints.
| OAR | Dose limitation | End point | Rate (%) |
|---|---|---|---|
| Spinal cord | Dmax = 50 | Myelopathy | 0.2 |
| Spinal cord | Dmax = 60 | Myelopathy | 6 |
| Spinal cord | Dmax = 69 | Myelopathy | 50 |
| Whole liver | Mean dose 30-32 | Classical RILD | <5 |
| Whole liver | Mean dose <42 | Classical RILD | <50 |
| Small intestine | V45 < 195 cc (entire potential space within peritoneal cavity) | Grade >= 3 acute toxicity | <10 |
| Heart | Mean dose <26 (pericardium) | Pericarditis | <15 |
| Heart | V30 < 46% (pericardium) | Pericarditis | <15 |
| Heart | V25 < 10% (whole heart) | Long-term cardiac mortality | <1 |
| Bilateral whole kidneys | Mean dose <15-18 | Clinically relevant renal dysfunction | <5 |
| Bilateral whole kidneys | Mean dose <28 | Clinically relevant renal dysfunction | <50 |
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.9)
La discusión final alinea la radioquimioterapia adyuvante con los estudios aleatorizados citados en el capítulo. La lectura práctica es selectiva: márgenes comprometidos, enfermedad pT3 o pT4 y resecciones inferiores a D2 son los escenarios en los que la adición de radioterapia parece más justificable. En ARTIST, los pacientes con ganglios positivos se beneficiaron de la radioterapia, pero esa señal no se reprodujo en ARTIST II.
Adjuvant and perioperative treatment approaches summarized in the chapter
The chapter closes by aligning adjuvant chemoradiotherapy with the main randomized data sets cited in the text. The extraction of this table is partially degraded in the prompt, but the entries below follow the reported trial names, arms, survival figures, hazard ratios, and notes visible in the extracted pages.
| Trial | Year | N | Arms | OS (%) | Median OS | HR / P | Notes |
|---|---|---|---|---|---|---|---|
| INT0116 | 2001, updated 2012 [8] | 556 | 1: Surgery 2: Surgery -> Adjuvant CRT (5FU) |
41 vs 50 (3-year) | 27 vs 36 months | HR 1.32; P = 0.005 | D2 surgery in 10%; all R0 resection |
| ARTIST | 2012, 2015 [9] | 458 | 1: D2 -> Adjuvant chemo, XP x 6 cycles 2: D2 -> XP x 2 cycles -> CRT -> XP x 2 cycles |
73 vs 75 (5-year) | NR vs NR | NS | No OS difference; improved DFS for node-positive disease and intestinal histology |
| ARTIST II | 2021 [10] | 546 | 1: D2 -> S1 for 1 year 2: D2 -> SOX x 6 months 3: D2 -> SOX x 2 months -> RT -> SOX x 4 months (SOXRT) |
NR | NR | S1 vs SOX: HR 0.692, P = 0.042 SOX vs SOXRT: HR 0.724, P = 0.074 |
3-year DFS 73, 74, and 65 |
| MAGIC | 2006 [11] | 503 | 1: Surgery 2: Chemo (ECF) -> Surgery -> Chemo |
23 vs 36 (5-year) | 18 vs 30 months | HR 0.75; P = 0.009 | Perioperative ECF |
| CRITICS | 2018 [12] | 788 | 1: Chemo (ECF or ECX) -> Surgery -> Chemo 2: Chemo -> Surgery -> Adjuvant CRT |
41 vs 41 (5-year) | 43 vs 37 months | NS | No difference in OS or toxicity |
| ACTS-GC | 2007 [13] | 1059 | 1: Surgery 2: Surgery -> Chemo (S1) |
70 vs 80 (3-year) | NR | HR 0.68; P = 0.003 | East Asian population |
| CLASSIC | 2012 [14] | 1035 | 1: Surgery 2: Surgery -> Chemo (CapeOx) |
70 vs 78 (5-year) | NR | HR 0.66; P = 0.0015 | China, South Korea, Taiwan |
| TOPGEAR | Recruiting | NR | 1: Chemo -> Surgery 2: ChemoRT -> Surgery |
NR | NR | NR | Neoadjuvant strategy under study |
| CRITICS II | Recruiting | NR | 1: Chemo -> Surgery 2: ChemoRT -> Chemo -> Surgery 3: CRT -> Surgery |
NR | NR | NR | Recruitment ongoing |
Abbreviations: OS overall survival, DFS disease-free survival, HR hazard ratio, NS not statistically significant, NR not reported, ECF epirubicin/cisplatin/5-FU, ECX epirubicin/cisplatin/xeloda, S1 tegafur/gimeracil/oteracil.
Source: Target Volume Delineation and Field Setup: A Practical Guide for Conformal and Intensity-Modulated Radiation Therapy, 2nd Edition (Table 15.10)
Para situar estos campos posoperatorios dentro de un marco más amplio, vuelva al Target Volume Delineation and Field Setup – Complete Clinical Guide. Si busca una comparación fuera del abdomen superior, nuestro artículo sobre carcinoma de orofaringe muestra cómo cambia la lógica del delineado según el sitio primario.

