Terapia con Haces de Iones: Por Qué Monte Carlo Marca la Diferencia
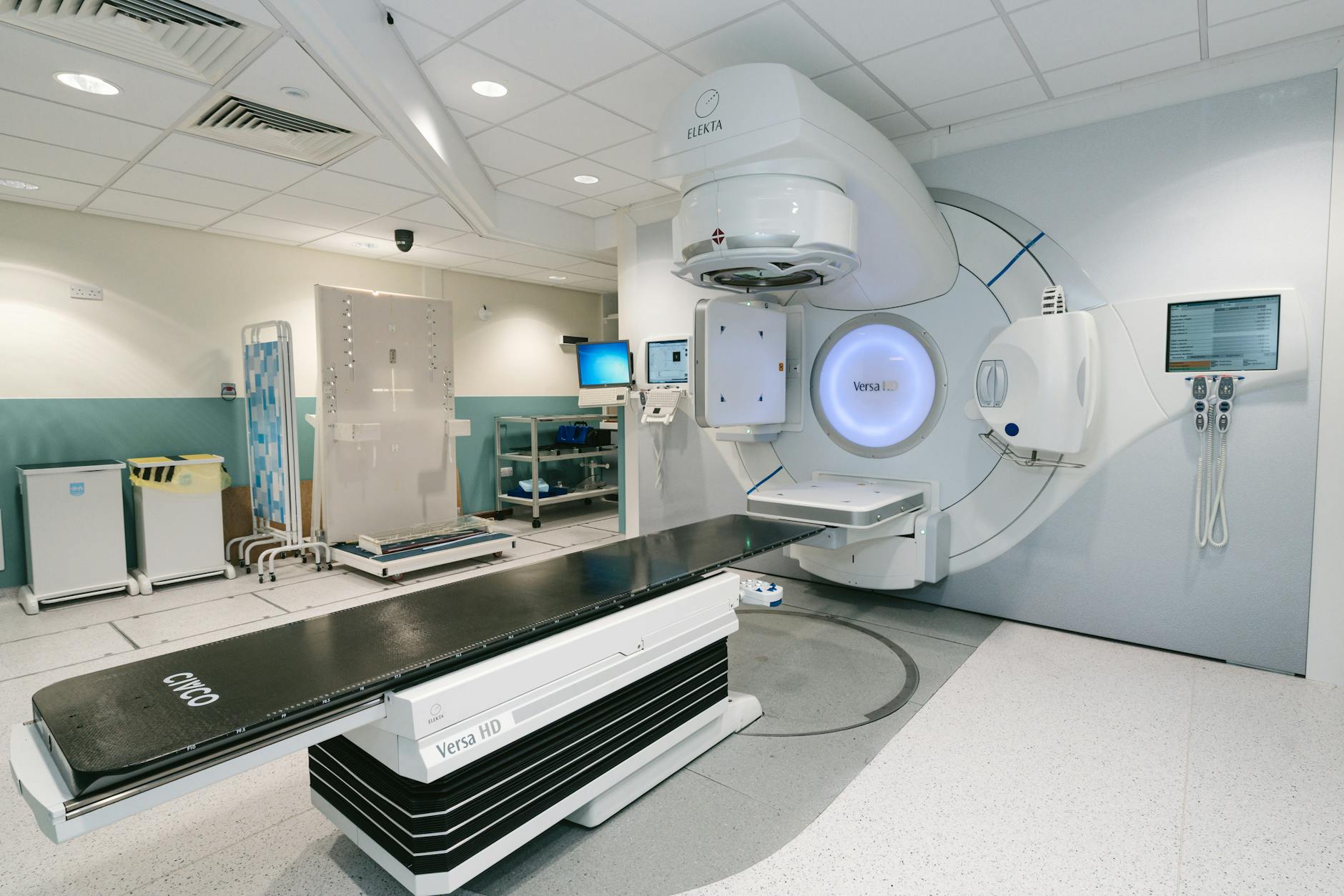
La terapia con haces de iones representa uno de los avances más sofisticados de la radioterapia moderna. A diferencia de los fotones, las partículas cargadas pesadas depositan su energía de forma altamente localizada, con un pico de Bragg pronunciado que permite concentrar la dosis en el tumor y respetar los tejidos sanos circundantes. Sin embargo, este mismo perfil de deposición de energía exige una precisión de cálculo que los algoritmos convencionales simplemente no pueden garantizar. Monte Carlo, con su capacidad para simular la física de transporte de partículas de forma estadísticamente rigurosa, se ha convertido en la herramienta de referencia para enfrentar estos desafíos.
Este artículo corresponde al cuarto de la serie dedicada a Monte Carlo en Radioterapia. Si aún no has revisado los fundamentos del método, te recomendamos comenzar por Fundamentos de Monte Carlo en Radioterapia, donde se establecen las bases estadísticas y físicas del método. Para una visión completa de la serie, consulta también nuestra Guía Completa de Monte Carlo en Radioterapia.
La discusión que sigue se centra en la entrega de haz de iones mediante escaneo activo — conocida por sus siglas en inglés como SIBD (Scanned Ion Beam Delivery) — y cubre tanto los iones ligeros más comunes en uso clínico, como protones y iones de carbono, como los desafíos específicos que cada uno plantea al modelado Monte Carlo.
Entrega de Haz de Iones por Escaneo Activo (SIBD)
El escaneo activo es una técnica dependiente del tiempo. A diferencia de los sistemas pasivos que modulan el haz mediante absorbentes físicos y colimadores, el SIBD utiliza imanes de deflexión para desplazar el haz en dos dimensiones, recorriendo la sección transversal del volumen blanco punto por punto, capa por capa. Esta estrategia elimina gran parte de la radiación secundaria generada por los dispositivos pasivos y permite conformar tridimensionalmente la distribución de dosis con un control sin precedentes.
Los rangos energéticos típicos en uso clínico abarcan de 60 a 250 MeV para protones, lo que corresponde a rangos en tejido de aproximadamente 30 a 380 mm. Para iones de carbono, los aceleradores operan entre 120 y 430 MeV/u, cubriendo rangos de 30 a 300 mm. La fuente de estos haces puede ser un sincrotrón, que ofrece la ventaja de variar directamente la energía extraída, o un ciclotrón de energía fija que requiere degradadores para ajustar el alcance. En ambos casos, la calidad del modelo Monte Carlo del sistema de entrega determina en última instancia la fidelidad dosimétrica del tratamiento.
Para blancos superficiales o proximales, se utilizan desplazadores de rango (range shifters), bloques de material de bajo número atómico que reducen la energía del haz antes de que entre al paciente. La boquilla (nozzle) del sistema — el componente final antes del paciente — tiene un equivalente en agua (WET, Water Equivalent Thickness) típico de 1 a 3 mm cuando no se emplean accesorios pasivos. Este detalle, aparentemente menor, tiene consecuencias importantes en el modelado, como se verá más adelante.
Descripción del Haz de Lápiz: Parámetros Energéticos y Ópticos
El elemento fundamental del escaneo activo es el haz de lápiz (pencil beam): un haz estrecho y monocrómático que se deposita sucesivamente en posiciones previamente calculadas por el sistema de planificación. Caracterizar este haz con precisión es el primer paso para cualquier modelo Monte Carlo de la cabeza de tratamiento.
Los parámetros que definen un haz de lápiz se dividen en dos categorías: energéticos y ópticos. Los parámetros energéticos son la energía media del haz y su dispersión energética. Los parámetros ópticos describen la geometría transversal del haz en el espacio de fase: tamaño, divergencia y emitancia.
La descripción formal del espacio de fase se hace a través de la elipse de fase, utilizando los parámetros de Twiss $\alpha$, $\beta$, $\gamma$ y la emitancia $\varepsilon$. La ecuación de la elipse en el espacio $(x, x’)$ — posición y ángulo — es:
$$\gamma x^2 + 2\alpha x x’ + \beta x’^2 = \varepsilon$$
con la restricción:
$$\beta\gamma – \alpha^2 = 1$$
En el punto de cintura del haz, donde la divergencia es mínima, $\alpha = 0$ y la emitancia se puede expresar directamente como:
$$\varepsilon = \pi \cdot \sigma_x \cdot \sigma_\theta$$
donde $\sigma_x$ es el tamaño del haz y $\sigma_\theta$ es su divergencia angular. La convención más habitual en física de haces define $A = 4\pi\varepsilon$, de modo que las varianzas del tamaño e inclinación del haz resultan:
$$\sigma_x^2 = \varepsilon \cdot \beta, \qquad \sigma_{x’}^2 = \varepsilon \cdot \gamma$$
Esta descripción formal no es un formalismo académico abstracto; tiene consecuencias directas y cuantificables en la distribución de dosis lateral. Un error en la estimación de la emitancia se traduce en errores en la penumbra lateral del haz y, en consecuencia, en una cobertura inadecuada del margen tumoral o en una sobredosis innecesaria de estructuras críticas adyacentes.
Propiedades de Escaneo y Geometría del Sistema
Además de las propiedades intrínsecas del haz, el modelado Monte Carlo debe incorporar la geometría del sistema de escaneo. El parámetro clave aquí es la distancia fuente-eje (SAD, Source-to-Axis Distance), que determina si el haz es geométricamente divergente o cuasi-paralelo al llegar al isocentro.
Algunos sistemas, especialmente los diseñados para tratar lesiones con geometrías complejas, utilizan una distancia SAD virtual (vSAD): el haz no diverge desde un punto físico real, sino que su geometría de escaneo equivale a una fuente virtual ubicada a una distancia calculada. Esta distinción es fundamental al construir el modelo Monte Carlo, ya que afecta directamente la distribución lateral de dosis en profundidad.
Entre los accesorios de boquilla más relevantes para el modelado figuran:
- Desplazador de rango (range shifter): Reduce la energía del haz para alcanzar blancos superficiales. Introduce dispersión energética y angular adicional que el modelo debe reproducir fielmente.
- Filtro de rizado (ripple filter): Utilizado principalmente con iones de carbono para homogeneizar la distribución de dosis longitudinal. Requiere una precisión de modelado del orden de 10 µm para reproducir correctamente el perfil de dosis resultante.
- Boquilla móvil (moving snout): Permite acercar el último componente activo al paciente, reduciendo la penumbra lateral para campos pequeños.
Cada uno de estos accesorios introduce modificaciones físicas al haz que los algoritmos analíticos describen de forma aproximada. Monte Carlo, al simular explícitamente las interacciones físicas dentro de cada componente, los modela de forma intrínsecamente más precisa.
Métodos de Modelado: Boquilla Completa y Salida de Boquilla
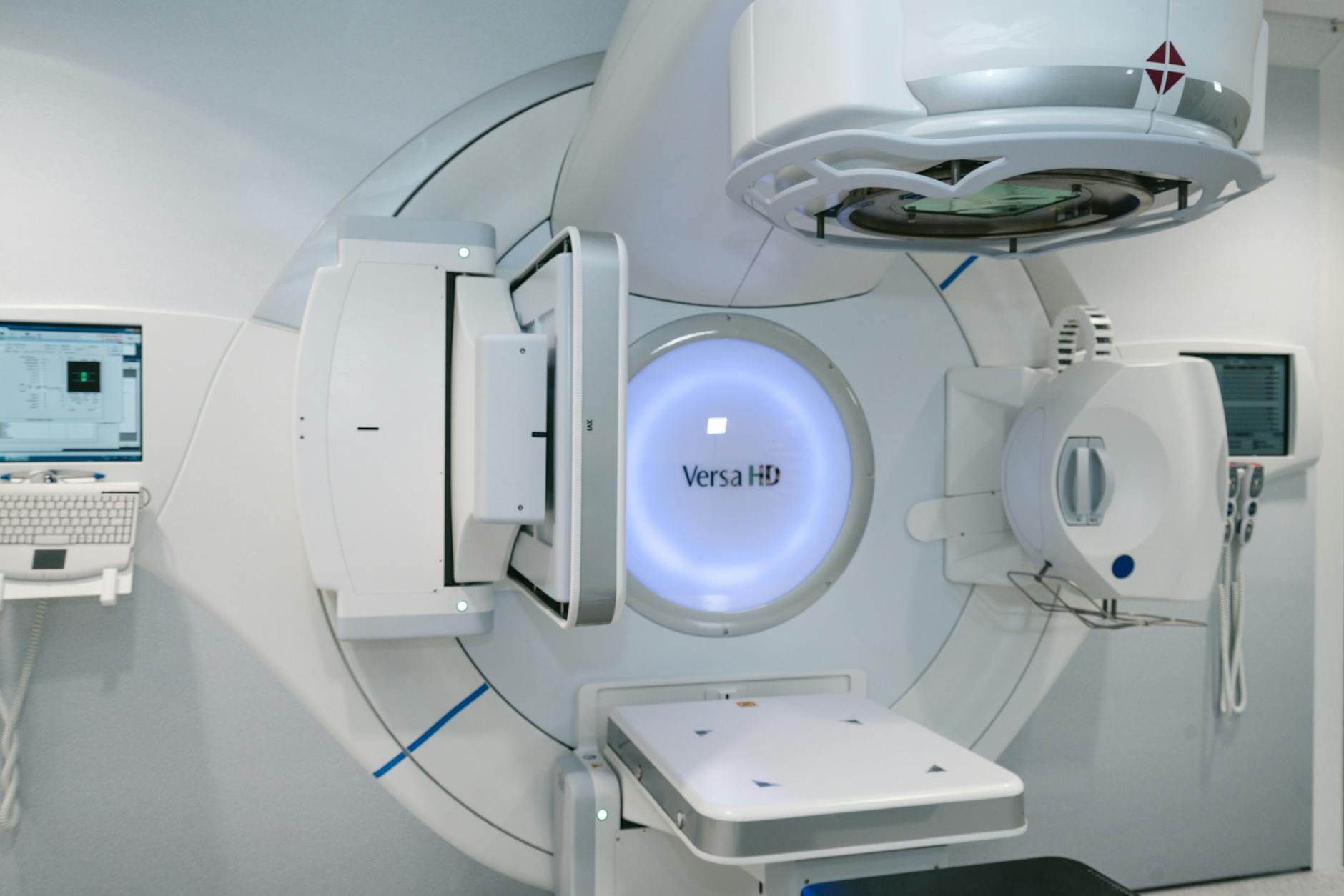
Existen dos filosofías principales para construir el modelo Monte Carlo de la cabeza de tratamiento: el método de boquilla completa (full-nozzle) y el método de salida de boquilla (nozzle exit). Cada uno tiene sus ventajas, limitaciones y requisitos de información.
Método de Salida de Boquilla
Desarrollado originalmente en el PSI (Paul Scherrer Institut) a principios de la década de 2000, este método prescinde de simular los componentes físicos de la boquilla. En cambio, caracteriza el haz directamente en el plano de salida de la boquilla mediante datos de comisionamiento medidos experimentalmente. La ventaja práctica es obvia: no se necesitan los planos de fabricación del acelerador, información que los fabricantes suelen proporcionar con restricciones.
La base matemática del método es el formalismo de Fermi-Eyges para la propagación del haz en el aire. La varianza lateral del haz en una posición $z$ a lo largo del eje del haz se expresa como:
$$\sigma_x^2(z) = A_{2,x} + 2z \cdot A_{1,x} + z^2 \cdot A_{0,x} + T \cdot z^3$$
donde los coeficientes $A_{0,x}$, $A_{1,x}$ y $A_{2,x}$ se obtienen del ajuste a medidas de perfil lateral a diferentes profundidades en agua, y el término $T \cdot z^3$ corresponde a la dispersión por múltiple Coulomb en el aire entre la boquilla y el paciente. La emitancia del haz puede recuperarse de estos coeficientes mediante:
$$M_x = \pi \sqrt{A_{0,x} \cdot A_{2,x} – A_{1,x}^2}$$
Una limitación inherente del método de salida de boquilla es que no modela las partículas secundarias generadas dentro de la boquilla. Sin embargo, estas secundarias representan menos del 0,5% de la dosis total en la mayoría de las configuraciones clínicas sin accesorios pasivos, por lo que la aproximación es aceptable para la mayoría de los escenarios de tratamiento estándar.
Método de Boquilla Completa
El método de boquilla completa simula explícitamente todos los componentes físicos de la línea de haz: monitores de dosis, cámaras de ionización, filtros, desplazadores de rango y la propia geometría de la boquilla. Este enfoque requiere acceso a los planos detallados del fabricante, pero ofrece a cambio una fidelidad física superior, especialmente cuando se utilizan accesorios que modifican significativamente el haz.
El grupo del MD Anderson Cancer Center ha desarrollado modelos de boquilla completa utilizando MCNPX para sistemas Hitachi, mientras que el centro MedAustron en Austria ha implementado modelos análogos para su sistema de haz convergente. Estos desarrollos han demostrado que la simulación explícita de la boquilla es necesaria cuando se emplean desplazadores de rango de gran espesor o cuando la geometría del haz es convergente en lugar de divergente.
En la práctica, la elección entre ambos métodos depende de la disponibilidad de información del fabricante y de los requerimientos de precisión de cada instalación. Para sistemas con boquillas simples y sin accesorios de campo complejo, el método de salida de boquilla ofrece una excelente relación entre precisión y esfuerzo de comisionamiento.
Receta de Modelado y Calibración del Sistema
El proceso de construcción de un modelo Monte Carlo clínico para SIBD sigue una secuencia bien definida. No se trata de un proceso genérico; cada instalación tiene su propia geometría de boquilla, su propio perfil energético y sus propias condiciones de entrega.
Proceso de Modelado Paso a Paso
| Etapa | Parámetros a determinar | Método |
|---|---|---|
| 1. Propiedades energéticas | Energía media, dispersión energética | Medida de curvas de Bragg en agua |
| 2. Propiedades ópticas | $\alpha$, $\beta$, $\gamma$, $\varepsilon$ (Twiss) | Perfiles laterales a múltiples profundidades |
| 3. Calibración N/MU | Factor dosis-unidades de monitor | Medida DAP y simulación MC |
| 4. Interpolación entre energías | Parámetros a energías intermedias | Interpolación de 8-27 energías modeladas |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
La calibración en unidades de monitor merece atención especial. El factor de calibración $N/MU(E)$ relaciona el número de partículas simuladas con las unidades de monitor entregadas clínicamente, y se determina comparando el producto dosis-área (DAP, Dose-Area Product) medido experimentalmente con el calculado por Monte Carlo:
$$\frac{N}{MU}(E) = \frac{DAP_{\text{medido}}}{DAP_{\text{simulado}}} \times N_{\text{sim}}$$
Esta calibración es específica de cada energía del haz. En la práctica, se modelan explícitamente entre 8 y 27 energías representativas y se interpolan los parámetros para las energías intermedias. La densidad de puntos de calibración debe ser suficiente para capturar las variaciones no lineales en los parámetros del haz, especialmente en los extremos del rango energético.
El Halo Nuclear en Haces de Protones
Una de las diferencias más relevantes entre los algoritmos analíticos de haz de lápiz y Monte Carlo en protonterapia es la modelización del halo nuclear. Cuando un haz de protones de energía clínica atraviesa materia, una fracción significativa de las partículas sufre interacciones nucleares inelásticas que producen protones secundarios, neutrones y fragmentos de baja energía. A 160 MeV, aproximadamente el 20% de los protones del haz original experimenta algún tipo de interacción nuclear antes de llegar al pico de Bragg.
El resultado es una distribución de dosis lateral que no puede describirse con un único componente gaussiano. La literatura reconoce tres componentes distintos:
- Núcleo (core): El componente gaussiano estrecho dominante, producido por los protones primarios que solo han sufrido dispersión de Coulomb múltiple.
- Halo: Una distribución gaussiana más ancha producida por protones secundarios de interacciones nucleares elásticas e inelásticas. Se extiende varios centímetros lateralmente del eje del haz.
- Aura: Un componente de muy baja dosis y gran extensión lateral, asociado a neutrones y partículas secundarias de alta energía.
Además de estos tres componentes, existe un efecto adicional denominado spray: la deposición de dosis difusa en regiones distantes del eje del haz producida por fragmentos y partículas secundarias. En profundidades intermedias — antes del pico de Bragg — puede observarse un incremento local de dosis denominado midrange bump, asociado a la acumulación de secundarias de baja energía.
La importancia cuantitativa del halo nuclear no es despreciable. Para un haz de protones de 252,7 MeV, la corrección por halo nuclear puede alcanzar el 8% de la dosis total en el pico de Bragg. Los algoritmos analíticos que no modelan este efecto sobreestiman la dosis puntual en el eje y subestiman la dosis en las regiones laterales, lo que puede resultar en una cobertura inadecuada del volumen blanco o en una subestimación de la dosis en órganos en riesgo adyacentes.
Fragmentación Nuclear en Haces de Carbono
Si la física del halo nuclear ya complica el modelado de protones, los iones de carbono presentan un desafío adicional de mayor magnitud: la fragmentación nuclear. A 290 MeV/u, aproximadamente el 40% de los iones de carbono del haz sufre algún tipo de interacción nuclear inelástica antes de depositar toda su energía. El porcentaje de fragmentación acumulada puede superar el 50% a lo largo de todo el recorrido en tejido.
El proceso de fragmentación produce una cascada de fragmentos con distintas cargas, masas, energías y rangos. Estos fragmentos — boro, berilio, litio, helio-4, helio-3, deuterio, protones y neutrones, entre otros — tienen características de transporte completamente diferentes al ion primario. Algunos tienen rangos más largos que el ion de carbono original, lo que genera una cola de dosis distal que se extiende más allá del pico de Bragg del carbono y que puede irradiar tejidos sanos en la región posterior al tumor.
Para modelar adecuadamente esta fragmentación, se utiliza un denominado modelo tricrómico (trichrome model) que divide los fragmentos en tres categorías según su número de masa, con parámetros ajustados a datos experimentales. La diferencia en la distribución de dosis calculada con y sin modelado adecuado de fragmentación puede alcanzar el 2,7% en términos de dosis media al volumen blanco, una diferencia clínicamente relevante considerando los objetivos de precisión dosimétrica de ±2% que se persiguen en protonterapia y terapia con iones pesados.
| Parámetro | Protones (160 MeV) | Carbono (290 MeV/u) |
|---|---|---|
| Fracción con interacciones nucleares | ~20% | ~40% |
| Fragmentación acumulada total | Baja (halo ~8% a 252,7 MeV) | Hasta 50% |
| Cola distal de dosis | Mínima | Significativa (fragmentos de mayor rango) |
| Error típico de PBA vs MC | ~5% | ~0,5% (sin accesorios) |
| Códigos MC recomendados | GEANT4, TOPAS, MCNP | FLUKA, PHITS, SHIELD-HIT |
Fuente: Monte Carlo Techniques in Radiation Therapy (2nd ed., CRC Press, 2022)
Un dato aparentemente paradójico en esta tabla merece explicación: el error relativo de PBA frente a MC es mayor para protones (~5%) que para carbono (~0,5%) en condiciones estándar sin accesorios. La razón es que la mayor rigidez magnética del carbono reduce su dispersión lateral por Coulomb múltiple, haciendo que el haz de carbono sea más «limpio» geométricamente. Sin embargo, cuando se introducen accesorios como desplazadores de rango, la situación se invierte dramáticamente.
Códigos Monte Carlo para Haces de Iones
La comunidad de terapia con iones pesados ha desarrollado y adoptado un conjunto de códigos Monte Carlo específicamente adaptados a las necesidades de esta modalidad. Cada código tiene sus fortalezas y sus áreas de aplicación preferencial.
FLUKA es el código de referencia en varios de los centros europeos más importantes, incluyendo el Heidelberger Ionenstrahl-Therapiezentrum (HIT) en Alemania y el CNAO (Centro Nazionale di Adroterapia Oncologica) en Italia. Su modelo de interacciones nucleares para iones pesados es especialmente robusto y ha sido validado extensamente contra datos experimentales.
GEANT4 — frecuentemente utilizado a través del entorno de usuario GATE, desarrollado específicamente para aplicaciones médicas — es la base del sistema de planificación de MedAustron en Austria. El proyecto TOPAS (TOol for PArticle Simulation), construido sobre GEANT4, ha facilitado enormemente el uso de este motor de simulación en centros clínicos sin experiencia avanzada en programación.
PHITS (Particle and Heavy Ion Transport code System) y SHIELD-HIT son alternativas utilizadas principalmente en centros de investigación, con modelos de fragmentación nuclear específicamente ajustados para aplicaciones de iones pesados.
Para aplicaciones clínicas donde el tiempo de cálculo es un factor limitante, se han desarrollado códigos Monte Carlo adaptados (fast MC): VMCPRO, MCSQUARE y FRED. Estos códigos implementan aproximaciones que aceleran el cálculo manteniendo una precisión suficiente para uso clínico, reduciendo los tiempos de cálculo de horas a minutos en hardware convencional.
Integración con Sistemas de Planificación de Tratamiento
La integración de Monte Carlo en los sistemas de planificación de tratamiento (TPS) para terapia con iones presenta desafíos técnicos considerables. El tiempo de cálculo de un Monte Carlo completo para un plan clínico típico — con múltiples campos y miles de spots de haz de lápiz — puede superar varios minutos incluso en servidores de alto rendimiento. Para uso clínico rutinario, esto ha impulsado el desarrollo de los códigos rápidos mencionados anteriormente.
La comparación sistemática entre Monte Carlo y los algoritmos analíticos de haz de lápiz revela diferencias que dependen fuertemente de la configuración del tratamiento. En condiciones estándar sin accesorios pasivos, las diferencias son moderadas: aproximadamente 5% para protones y 0,5% para carbono. Sin embargo, esta situación cambia radicalmente cuando se introducen desplazadores de rango de gran espesor.
Un ejemplo bien documentado ilustra la magnitud del problema: con un desplazador de rango de 7,5 cm combinado con un espacio de aire de 31,5 cm entre el desplazador y la superficie del paciente, el algoritmo PBA puede cometer errores de hasta el 10% en la dosis calculada. Monte Carlo, al simular explícitamente la dispersión adicional introducida por el desplazador y la propagación del haz en el aire, calcula correctamente el perfil lateral resultante.
Para el artículo específico sobre el cálculo de dosis Monte Carlo en el paciente, te recomendamos revisar Cálculo de Dosis Monte Carlo en el Paciente, donde se desarrollan en detalle los métodos de conversión de imagen CT y las incertidumbres asociadas al transporte de partículas en tejidos heterogéneos.
Aplicaciones Avanzadas: Diseño de Líneas de Haz y Terapia Guiada por RM
Más allá del cálculo de dosis clínico, Monte Carlo desempeña un papel central en el diseño y la optimización de las líneas de haz de nuevas instalaciones. El diseño de una boquilla para SIBD implica decisiones sobre la posición y tipo de monitores de dosis, la geometría de los imanes de escaneo, la distancia SAD y la selección de materiales. Cada una de estas decisiones afecta la calidad del haz entregado al paciente, y validar estas decisiones experimentalmente en una instalación que aún no existe requiere simulación Monte Carlo.
Una aplicación emergente de particular interés es la terapia con iones ligeros guiada por resonancia magnética (MRI-guided Light Ion Beam Therapy, LIBT). La integración de un sistema de RM con un acelerador de iones plantea desafíos únicos: el campo magnético del escáner de RM afecta directamente a la trayectoria del haz de iones, modificando su dispersión lateral y, en cierta medida, el perfil de dosis. Modelar correctamente esta interacción requiere un Monte Carlo capaz de simular el transporte de partículas en campos magnéticos externos, una capacidad que GEANT4/GATE y FLUKA proporcionan de forma nativa.
Incertidumbres en Monte Carlo para Haces de Iones
Ninguna discusión sobre Monte Carlo para haces de iones estaría completa sin abordar sus fuentes de incertidumbre. A diferencia de la incertidumbre estadística, que se puede reducir aumentando el número de historias simuladas, las incertidumbres sistemáticas son más difíciles de cuantificar y controlar.
Las principales fuentes de incertidumbre sistemática en Monte Carlo para iones son:
- Modelos de interacciones nucleares: Las secciones eficaces de fragmentación nuclear para iones intermedios (carbono, oxígeno) no están tan bien determinadas experimentalmente como las de protones. Los diferentes códigos utilizan modelos distintos, lo que puede producir diferencias de dosis no despreciables en la cola distal del pico de Bragg.
- Conversión CT-densidad: La conversión de unidades Hounsfield a poder de frenado relativo introduce una incertidumbre de rango de aproximadamente 1-2 mm en tejidos blandos y mayor en hueso.
- Parámetros del haz de entrada: Las incertidumbres en los parámetros ópticos y energéticos del haz de lápiz se propagan directamente al cálculo de dosis.
- Modelo geométrico de la boquilla: Para el método de boquilla completa, las tolerancias de fabricación de los componentes físicos introducen incertidumbres que deben ser caracterizadas experimentalmente.
Monte Carlo en el Contexto Clínico: Lo que el Físico Médico Necesita Saber
Desde la perspectiva de la práctica clínica diaria en un centro de terapia con iones, Monte Carlo no es una herramienta de investigación reservada a los físicos teóricos. Es — o debería ser — un componente integral del proceso de aseguramiento de calidad y del flujo de trabajo de planificación de tratamiento.
Para el comisionamiento inicial de un nuevo sistema de entrega, Monte Carlo proporciona la validación más rigurosa disponible de los parámetros del modelo TPS. Comparar las distribuciones de dosis calculadas por Monte Carlo con las medidas dosimétricas en fantoma de agua permite identificar discrepancias en los parámetros del modelo antes de que se traduzcan en errores dosimétricos en el paciente.
Para casos clínicos complejos — tumores de base de cráneo adyacentes al tronco encefálico, lesiones oculares, pediatría — donde el margen de error tolerable es mínimo, el cálculo Monte Carlo de verificación independiente del plan aprobado con PBA puede revelar diferencias que, en algunos casos, llevan a modificar el plan de tratamiento.
El artículo sobre Monte Carlo para Haces Fotónicos en Radioterapia ofrece una perspectiva comparativa útil sobre cómo se implementan estos mismos principios en el contexto más familiar de la radioterapia con fotones.
Perspectivas Futuras y Tendencias en Desarrollo
El campo de Monte Carlo para haces de iones está en rápida evolución. Tres tendencias principales marcan la dirección de los próximos años.
La primera es la aceleración del cálculo mediante hardware especializado. Las unidades de procesamiento gráfico (GPU) permiten paralelizar masivamente las simulaciones Monte Carlo, reduciendo los tiempos de cálculo de horas a segundos para planes clínicos típicos. Varios grupos de investigación han demostrado implementaciones GPU de GATE y de códigos MC rápidos que abren la puerta al Monte Carlo en tiempo real durante la verificación del plan.
La segunda tendencia es la integración de Monte Carlo en los flujos de trabajo de radioterapia adaptativa. Los tratamientos adaptativos requieren recalcular el plan sobre imágenes del día del tratamiento, lo que multiplica el número de cálculos necesarios.
La tercera es la aplicación de Monte Carlo al cálculo de efectividad biológica relativa (EBR). Para iones de carbono, la EBR varía significativamente con la posición dentro del campo, dependiendo del espectro local de LET (Linear Energy Transfer). Monte Carlo proporciona directamente los espectros de LET necesarios para los modelos biofísicos como el LEM (Local Effect Model) o el MKM (Microdosimetric Kinetic Model), con una fidelidad que los algoritmos analíticos solo pueden aproximar.
Conclusiones: Monte Carlo como Estándar de Referencia para Iones
La terapia con haces de iones representa el límite más exigente de la dosimetría computacional en radioterapia. La combinación de interacciones nucleares complejas, halo de dosis lateral, fragmentación de iones pesados y sensibilidad a la geometría de entrega crea un escenario donde los algoritmos analíticos producen errores sistemáticos que pueden tener consecuencia clínica.
Monte Carlo no es perfecto — sus propias incertidumbres de modelo y los tiempos de cálculo siguen siendo limitaciones reales — pero proporciona el marco físico más completo disponible para describir el transporte de partículas cargadas pesadas en materia. Para el físico médico que trabaja en terapia con iones, comprender los fundamentos del modelado Monte Carlo de la cabeza de tratamiento, los métodos de calibración y las fuentes de incertidumbre no es una opción académica: es parte de la competencia profesional necesaria para operar estos sistemas de forma segura y eficaz.
Para profundizar en los aspectos de garantía de calidad y verificación de planes con Monte Carlo en protonterapia, consulta el artículo Protones y QA: Monte Carlo en la Práctica, donde se detallan los protocolos de medida y los criterios de aceptación recomendados para el comisionamiento de sistemas de protonterapia.
Este artículo forma parte de la serie sobre Monte Carlo en Radioterapia. Para acceder a todos los artículos de la serie y a recursos adicionales, visita la Guía Completa de Monte Carlo en Radioterapia.